时间:2019-05-30 02:59:28
1、选择题 下列关于甲、乙、丙、丁四幅图说法正确的是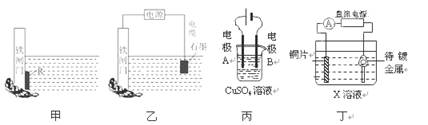
A.装置甲中对于铁闸门的保护用的是“牺牲阳极的阴极保护法”,焊接在铁闸上的金属R可以是锡块
B.装置乙中对于铁闸门的保护采用的是“外加电流的阴极保护法”,铁闸门应与直流电源的负极相连
C.装置丙可实现电解精炼铜,电极A的材料用纯铜,电极B的材料用粗铜
D.装置丁可实现镀铜,铜片接在电源的正极,待镀金属接在电源的负极,X溶液应用含有待镀金属阳离子的溶液
2、选择题 以惰性电极电解一定浓度的CuSO4溶液,通电一段时间后,向所得的溶液中加入0.1mol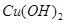 ,恰好恢复到电解前的pH和浓度,则电解过程中转移的电子的物质的量为:
,恰好恢复到电解前的pH和浓度,则电解过程中转移的电子的物质的量为:
A.0.1mol
B.0.2mol
C.0.3mol
D.0.4mol
3、填空题 氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
依据上图,完成下列填空:
(1)与电源负极相连的电极附近,溶液pH值(选填:不变、升高或下降),与电源正极相连的电极叫?极,检验该极上产物的方法是?。
(2)写出电解饱和食盐水的化学方程式?。
(3)如果粗盐中SO 含量较高,必须添加钡式剂除去SO
含量较高,必须添加钡式剂除去SO ,该钡试剂可以是(选填A.B.c,多选扣分)?
,该钡试剂可以是(选填A.B.c,多选扣分)?
A.Ba(OH)2? B.Ba(NO3)2? C.BaCl2?
(4)判断钡试剂已经过量的方法是?。
(5)为有效除去Ca2+、Mg2+、SO ,加入试剂的合理顺序为(选填a,b,c多选扣分)
,加入试剂的合理顺序为(选填a,b,c多选扣分)
A.先加NaOH溶液,后加Na2CO3溶液,再加钡试剂?
B.先加NaOH溶液,后加钡试剂,再加Na2CO3溶液?
C.先加钡试剂,后加NaOH溶液,再加Na2CO3溶液
(6)为检验精盐纯度,需配制150 mL0.2 mol/LNaCl(精盐)溶液,下图是该同学转移溶液的示意图,图中的错误是?。
4、填空题 (16分)如图所示,通电5 min后,电极5的质量增加了2.16 g,回答:
(1)电源:a是________极,C池是________池。
A池阳极电极反应式为__________________,阴极电极反应式为__________________。
C池阳极电极反应式__________________,阴极电极反应式为_____________________。
(2)如果B槽中共收集到224 mL气体(标准状况),且溶液体积为200 mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为______________________。
(3)如果A池溶液也是200 mL(电解过程中溶液体积不变),则通电后,溶液的pH为[________。
5、选择题 按如图所示装置进行下列不同的操作,说法不正确
的是?(?)
A.铁腐蚀的速度由大到小的顺序是:只接通K1>只
闭合K3>都断开>只闭合K2
B.只接通K1,一段时间后,U形管中出现白色沉淀
C.只接通K2,U形管左、右两端液面均下降
D.先只接通K1,一段时间后,漏斗液面上升,然后再
只接通K2,漏斗液面下降