时间:2019-05-30 02:40:58
1、选择题 铁在等物质的量浓度下列溶液中被腐蚀时由快到慢的顺序是 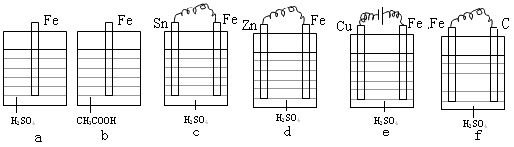
[? ]
A、e>d>a>b>c>f
B、e>f>c>a>b>d
C、e>c>f>a>b>d
D、e>f>d>a>b>c
2、选择题 下列有关金属腐蚀与防护的说法,正确的是
[? ]
A.纯银器表面在空气中因发生电化学腐蚀渐渐变暗
B.当镀锌铁制品的镀层破损时,镀层不再对铁制品起保护作用
C.在空气与水面交接处的钢柱,比在水下部分的钢柱容易腐蚀
D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀
3、填空题 (15分)填写下列空白:
(1)Fe(OH)3胶体呈红褐色,插入两个惰性电极,通直流电一段时间,阴极附近的颜色逐渐变深,这种现象叫______________。
(2)强光通过Fe(OH)3胶体,可看到光带,这种现象叫________________。
(3)淀粉与食盐的混合液放在肠衣(半透膜)中,并把它悬挂在盛有蒸馏水的烧瓶里,从而使淀粉与食盐分离,这种方法_______________。
(4)Fe(OH)3胶体加硅酸胶体,胶体变得浑浊,这是发生了____________。
(5)已知冰的熔化热为6.0 kJ/mol,冰中氢键键能为20 kJ/mol,假设1 mol冰中有2 mol 氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中_____%的氢键
4、选择题 在下列装置中(都盛有0.1mol/L H2SO4溶液)Zn片腐蚀最快的是?(?)
5、选择题 钢铁在潮湿的空气中会被腐蚀,发生的原电池反应为:2Fe+2H2O+O2 = 2Fe2++4OH-。以下说法正确的是
[? ]
A.负极发生的反应为:Fe-2e-=Fe2+
B.正极发生的反应为:2H2O+O2+2e-=4OH-
C.原电池是将电能转变为化学能的装置
D.钢柱在水下部分比在空气与水交界处更容易腐蚀