时间:2018-03-17 08:20:08
1、选择题 已知NaHSO4在水中的电离方程式为NaHSO4 Na++H++S。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。对于该溶液,下列叙述中不正确的是( )
Na++H++S。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。对于该溶液,下列叙述中不正确的是( )
A.该温度下加入等体积pH=12的NaOH溶液可使反应后的溶液恰好呈中性
B.水电离出来的c(H+)=1×10-10 mol・L-1
C.c(H+)=c(OH-)+c(S)
D.该温度高于25 ℃
参考答案:C
本题解析:某温度下,pH=6的蒸馏水,KW=1×10-12,NaHSO4溶液的pH为2,c(H+)=1×10-2 mol・L-1,pH=12的NaOH溶液,c(OH-)="1" mol・L-1,反应后的溶液呈碱性。由NaHSO4 Na++H++S和H2O
Na++H++S和H2O H++OH-可知C正确。
H++OH-可知C正确。
考点:水的电离、溶液的pH
本题难度:一般
2、选择题 已知碳酸、亚硫酸、次氯酸的平衡常数如下表: 下列反应的离子方程式书写正确的是
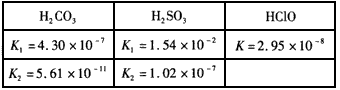
[?]
参考答案:B
本题解析:
本题难度:一般
3、填空题 (6分)(1)体积相同,浓度均为0.2 mol/L的盐酸和CH3COOH溶液,分别加水稀释10倍,溶液的pH分别变成m和n,则m与n的关系为?。
(2)体积相同,浓度均为0.2mo l/L的盐酸和CH3COOH溶液,分别加水稀释m倍、n倍,溶液的pH都变成3,则m与n的关系为?。
l/L的盐酸和CH3COOH溶液,分别加水稀释m倍、n倍,溶液的pH都变成3,则m与n的关系为?。
(3)体积相同,pH均等于13的氨水和NaOH溶液,分别加水稀释m倍、n倍,溶液的pH都变成9,则m与n的关系为?。
参考答案:(6分)(1) m<n?(2) m>n? ( 3) m>n
3) m>n
本题解析:略
本题难度:一般
4、选择题 MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如图所示。下列叙述中错误的是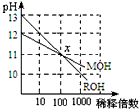
[? ]
A.ROH是一种强碱
B.在x点,c(M+) =c(R+)
C.在x点,ROH完全电离
D.稀释前,c(ROH)=10c(MOH)
参考答案:D
本题解析:
本题难度:一般
5、选择题 高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大。以下是某温度下这四种酸在冰醋酸中的电离常数:
| 酸 | HClO4 | H2SO4 | HCl | HNO3 |
| Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
 2H++S
2H++S参考答案:C
本题解析:从H2SO4的Ka可以看出,强酸在冰醋酸中电离受到抑制,多元酸分步电离,并非完全电离。
本题难度:一般