ʱ��:2018-03-17 08:18:40
1��ѡ���� �봿ˮ�ĵ������ƣ�Һ���д��������ĵ��룺2NH3?NH2-+NH4+�ݴ��жϣ����������в���ȷ���ǣ�������
A��Һ���к���?NH3��NH4+��NH2-?������
B��һ���¶��£�Һ����?c?��NH4+?����?c?��NH2-?���ij˻�Ϊ��ֵ
C��Һ���ĵ���ﵽƽ��ʱ��c?��NH3?��=c?��NH4+?��=c?��NH2-?��
D��ֻҪ�������������ʣ�Һ����c?��NH4+?��=c?��NH2-?��
�ο��𰸣�A��Һ�������д��ڵ���ƽ�⣬����Һ���к���?NH3��NH4+��NH2-?�����ӣ���A��ȷ��
B��Һ����?c?��NH4+?����?c?��NH2-?���ij˻�ֻ���¶��йأ�����Һ��Ũ���أ�����ֻҪ�¶�һ����Һ����?c?��NH4+?����?c?��NH2-?���ij˻�Ϊ��ֵ����B��ȷ��
C��Һ���ĵ��������ģ�����Һ������ﵽƽ��״̬ʱ��c?��NH4+?��=c?��NH2-?����c?��NH3?������C����
D��ֻҪ���ƻ������ӵĵ���ƽ�⣬Һ���������NH4+?��NH2-?�����ʵ�������ȣ���Ϊ��Һ�������ȣ�����c?��NH4+?��=c?��NH2-?������D��ȷ��
��ѡC��
���������
�����Ѷȣ���
2��ѡ���� ����ʵ������в������������Ӧ��ͼ����ȷ���ǣ�������
A��NaAlO2��Һ�м�������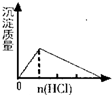
B��SO2����ͨ����ˮ��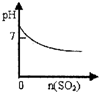
C��pH=2�Ĵ�����������Һ�ֱ��ˮϡ��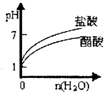
D������ͨ�������Һ��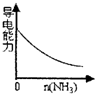
�ο��𰸣�A����NaAlO2��Һ�м������ᣬ������Ӧ�ֱ�ΪAlO2-+H++H2O�TAl��OH��3����Al��OH��3��+3H+�TAl3++3H2O����Ӧ��ʼʱ�г������ɣ�Ȼ������ܽ⣬��A��ȷ��
B��SO2����ͨ����ˮ�У�������ӦBr2+SO2+2H2O�TH2SO4+2HBr����Ӧ����Һ������ǿ��pH��С������ˮ��Һ�����ԣ���ʼʱpH��7����B����
C������Ϊ���ᣬ��ˮϡ��ʱ��һ�����룬pH�仯������С����������ôϡ�ͣ���Һ�������ԣ������ܳʼ��ԣ���C����
D������ͨ�������Һ�У���Ӧ����ǿ����ʴ���泥���Һ����������ǿ����D����
��ѡA��
���������
�����Ѷȣ�һ��
3��ѡ���� ��֪25 ��ʱ�й�����ĵ���ƽ�ⳣ�����±�:
| ���� | CH3COOH | HCN | H2CO3 |
| ����ƽ�ⳣ��(25 ��) | 1.8��10-5 | 4.9��10-10 | K1=4.3��10-7 K2=5.6��10-11 |
�ο��𰸣�D
���������A������c(Na+)��c(CN-),����Һ�е���غ�֪c(H+)��c(OH-),����a���ܵ��ڻ�С��b,A���;����������μ�ˮ,��Һ�ĵ�������������С,���������,pH�ȼ�С������,B���;C����û��˵������Һ�����ʵ���Ũ��,�����Ƚ�,C���;�������غ��:c(OH-)=c(CH3COOH)+c(H+),D����ȷ��
�����Ѷȣ�һ��
4��ѡ���� 25��ʱ����0.1mol��L��1��ˮ��Һ��ˮϡ�ͣ�������ֵ������
A��c(OH��)
B��pH
C��c(NH4+)/c(NH3��H2O)
D��c(H+)��c(OH��)
�ο��𰸣�C
����������ڰ�ˮ��Һ�м�ˮϡ�ͣ��ٽ�NH3��H2O�ĵ��룺NH3��H2O NH4++OH-��c(OH��)��С��pH��С����Kw=c(H+)��c(OH��)���䣻��c(NH4+)/c(NH3��H2O)��n(NH4+)/n(NH3��H2O)����ѡC��
NH4++OH-��c(OH��)��С��pH��С����Kw=c(H+)��c(OH��)���䣻��c(NH4+)/c(NH3��H2O)��n(NH4+)/n(NH3��H2O)����ѡC��
�����Ѷȣ�һ��
5������� ��֪25��ʱ����������ʵĵ���ƽ�ⳣ���������±���
| ��ѧʽ | CH3COOH | H2CO3 | HClO | |
| ƽ�ⳣ�� | Ka=1.8��10-5 | Ka1=4.3��10-7 | Ka2=5.6��10-11 | Ka=3.0��10-8 |
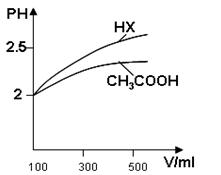
�ο��𰸣���1��a��d��c��b��(����)��
�������£ģ����֣�
��3�����ڣ�2�֣� ϡ����ͬ������һԪ
��HX��PH�仯��CH3COOH������ǿ������ƽ�ⳣ����2�֣�
��4��9.9��10-7��3�֣�? 18��3�֣�
�����������
�����Ѷȣ�һ��