时间:2018-03-17 08:04:40
1、填空题 (8分)
I.已知在25℃时,HF、HCN和H2CO3的的电离平衡常数如表所示:
(1)写出碳酸的第一级电离平衡常数表达式:K1= 。
(2)①往Na2CO3溶液中加入足量HF溶液,发生反应的离子方程式:
②往NaCN溶液中通入少量CO2,发生反应的离子方程式:
II. 用电解法制取金属镁时,需要无水氯化镁。在干燥的HCl气流中加热MgCl2・6H2O时,能得到无水MgCl2,其原因是 。
参考答案:)I. (1)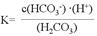 (2分)
(2分)
(2)①2HF+CO32-=2F-+H2O+CO2↑ (2分)②CN-+H2O+CO2= HCN+HCO3- (2分)
II. 在干燥的HCl气流中,抑制了MgCl2的水解,且带走了MgCl2・6H2O受热产生的水蒸气。(2分)
本题解析:(1)碳酸是二元弱酸,分别电离,碳酸的第一级电离平衡常数表达式: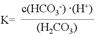 ;(2)①由于酸性HF>H2CO3,所以往Na2CO3溶液中加入足量HF溶液,发生反应的离子方程式2HF+CO32-=2F-+H2O+CO2↑;②由于酸性:H2CO3> HCN> HCO3- ,往NaCN溶液中通入少量CO2,发生反应的离子方程式是CN-+H2O+CO2= HCN+HCO3-;II. 用电解法制取金属镁时,需要无水氯化镁。在干燥的HCl气流中加热MgCl2・6H2O时,能得到无水MgCl2,其原因是在干燥的HCl气流中,抑制了MgCl2的水解,且带走了MgCl2・6H2O受热产生的水蒸气,从而得到无水MgCl2。
;(2)①由于酸性HF>H2CO3,所以往Na2CO3溶液中加入足量HF溶液,发生反应的离子方程式2HF+CO32-=2F-+H2O+CO2↑;②由于酸性:H2CO3> HCN> HCO3- ,往NaCN溶液中通入少量CO2,发生反应的离子方程式是CN-+H2O+CO2= HCN+HCO3-;II. 用电解法制取金属镁时,需要无水氯化镁。在干燥的HCl气流中加热MgCl2・6H2O时,能得到无水MgCl2,其原因是在干燥的HCl气流中,抑制了MgCl2的水解,且带走了MgCl2・6H2O受热产生的水蒸气,从而得到无水MgCl2。
考点:考查弱酸的电离平衡常数的应用、离子方程式的书写及盐的水解对物质制取条件的影响的知识。
本题难度:一般
2、填空题 下图为常温下向25mL 0.1 mol・L-1 MOH溶液中逐滴滴加0.2 mol・L-1HA溶液过程中溶液pH的变化曲线。
回答下列问题:
(1)上图能确定MOH为 (“强”或“弱”)碱,
理由是 。
(2)上图能确定HA为 (“强”或“弱”)酸,
理由是 。
(3)在D点时,溶液中c(A-)+c(HA) 2c(M+)。(填“>”、“<”或“=”)
参考答案:(1)强(2分);常温条件下水的离子积常数为10-14,0.1 mol・L-1 MOH溶液的pH=13,说明为强碱。(3分)[来源:91考试网ZXXK]
(2)弱(2分);若HA为强酸则在pH=7是刚好完 全反应,体积消耗HA12.5mL,而现在是13ml,说明生成的强碱弱酸盐。(3分)
(3)=(3分)
本题解析:略
本题难度:困难
3、选择题 常温下,下列有关叙述正确的是
A.在Na2CO3溶液中:2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
B.在pH=8的NaB溶液中 :c(Na+)-c(B
参考答案:
本题解析:
本题难度:一般
4、选择题 25℃时,向20 mL 0.2 mol/L H2A(某二元弱酸)溶液中滴加0.2 mol/L NaOH溶液,有关微粒的物质的量变化如下图(其中I代表H2A,II代表HA-,III代表A2-)?根据图示判断,下列说法中正确的是
A.当V(NaOH)=20mL时,所得溶液中:c(OH-)> c(H+)
B.当V(NaOH)=30mL时,所得溶液中:2c(H+) + c(HA-)+ 3c(H2A) = c(A2-) + 2 c(OH-)
C.当V(NaOH)=40mL时,所得溶液中:c(Na+)> c(A2-) >c(H+)> c(HA-) >c(OH-)
D.在NaHA溶液中:c(OH-)+2c(A2-) = c(H+)+2c(H2A)
参考答案:B
本题解析:A.当V(NaOH)=20mL时,发生反应:NaOH+H2A=NaHA+H2O。所得溶液是NaHA。由于HA-在溶液中存在电离作用和水解作用,电离产生H+使溶液显酸性,水解消耗H+,使溶液显碱性。由于此时溶液中c(H2A)< c(A2-),说明水解作用很弱,电离占优势,故(OH-)<c(H+),错误。B.当V(NaOH)=30mL时,所得溶液是NaHA、Na2A等浓度的混合溶液。根据图像可知c(HA-)< c(A2-),说明c(HA-)的电离程度大于c(A2-)的水解程度。溶液显酸性。根据物料守恒可得:2c(Na+)=3c(A2-)+ 3c(HA-)+3c(H2A)。根据电荷守恒可得c(H+)+ c(Na+)=c(OH-)+2 c(A2-)+c(HA-)。将第二个式子扩大2倍,与第一个式子相减,整理可得2c(H+) + c(HA-)+ 3c(H2A) = c(A2-) + 2 c(OH-),正确;C.当V(NaOH)=40mL时,酸碱恰好完全中和,产生Na2A。由于该盐是强碱弱酸盐,A2-发生水解反应而消耗,水电离产生的H+被消耗,最终当溶液中的水达到电离平衡时,c(OH-)> c(H+)。由于溶液中除了A2-、HA-水解产生OH-外,还存在水电离产生的OH-。所以c(OH-)> c(HA-) 。故溶液中离子浓度大小关系正确的是所得溶液中:c(Na+)> c(A2-) > c(OH-)> c(HA-)>c(H+),错误。
考点:考查酸碱发生中和反应时溶液中离子浓度大小比较的关系的知识。
本题难度:困难
5、选择题 已知某溶液中存在 ,
, ,
, 和
和 四种离子,其浓度大小有如下关系,其中可能的是( )
四种离子,其浓度大小有如下关系,其中可能的是( )
① ②
②
③ 且
且 ④
④
⑤
A.①④
B.③⑤
C.①②③
D.④⑤
参考答案:C
本题解析:①正确,此时溶质是氯化铵或氯化铵和氯化氢的混合液。②正确,应该是氯化铵和氯化氢的混合液。③符合电荷守恒,正确。④不符合电荷守恒c(H+)+c(NH4+)=c(OH-)+c(Cl-),不正确。氯化铵的水解程度是很小的,因此⑤不正确,答案选C。
本题难度:困难