时间:2018-03-17 07:48:43
1、填空题 (14分)(1)氨的合成是最重要的化工生产之一,工业上合成氨用的H2有多种制取的方法。用天然气跟水蒸气反应:CH4(g)+H2O(g)  CO(g)+3H2(g)。已知有关反应的能量变化如下图所示,则此制取H2反应的ΔH=____________。
CO(g)+3H2(g)。已知有关反应的能量变化如下图所示,则此制取H2反应的ΔH=____________。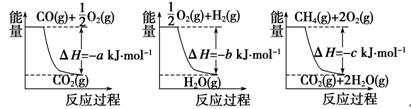
(2)已知通常状况下,每充分燃烧1gCO并恢复到原状态,会释放10KJ的热量。请写出表示CO燃烧热的热化学反应方程式: 。
(3)一种甲烷燃料电池是采用铂或碳化钨作为电极催化剂,在稀硫酸电解液中直接通入甲烷,同时向一个电极通入空气。此电池的负极电极反应式是________________________________________________。
(4)利用下图装置可以模拟铁的电化学防护。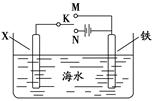
①若X为碳棒,为减缓铁的腐蚀,开关K应置于 处。假设海水中只有NaCl溶质,写出此时总离子反应方程式: 。
②若X为锌,开关K置于M处,该电化学防护法称为 。
写出铁电极处的电极反应式: 。
参考答案:(1)ΔH=(a+3b-c) kJ·mol-1 (2分)
(写成ΔH=+(a+3b-c) kJ·mol-1 或ΔH=-(c-a-3b) kJ·mol-1均正确漏写单位扣1分)
(2)CO(g)+1/2O2(g)=CO2(g) ΔH=-280KJ/mol (2分)
(无状态不得分;CO系数不为1不得分;漏单位扣1分。)
(3)CH4 -8e- + 2H2O = CO2 + 8H+ (2分)
(物质错漏不得分,系数错扣1分)
(4)①N(2分) 2Cl-+2H2O 2OH-+H2↑+Cl2↑ (2分)
2OH-+H2↑+Cl2↑ (2分)
(写成化学方程式不得分;系数、条件和箭头错总扣1分)
②牺牲阳极的阴极保护法 (2分) O2+2H2O+4e—=4OH— (2分)
本题解析:(1)三个反应的热化学方程式为:①CO(g)+1/2O2(g)=CO2(g) ΔH=-aKJ/mol, ②2H2(g)+O2(g)=2H2O(g) ΔH=-bKJ/mol,③CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-cKJ/mol,根据盖斯定律分析,三个反应应该①+3×②-③,所以反应热ΔH=(a+3b-c) kJ·mol-1。(2)1克一氧化碳的物质的量为1/28摩尔,所以每摩尔一氧化碳反应生成二氧化碳反应放出的热量为280KJ所以热化学方程式为:CO(g)+1/2O2(g)=CO2(g) ΔH=-280KJ/mol。(3)甲烷在原电池中左负极,在酸性条件下反应生成二氧化碳和水,电极反应为:CH4 -8e- + 2H2O = CO2 + 8H+。(4)①X为碳棒,减缓铁的腐蚀,需要将铁电解池的阴极,即连接N;电解氯化钠,反应生成氢氧化钠和氢气和氯气,离子方程式为:2Cl-+2H2O 2OH-+H2↑+Cl2↑。②X为锌,开关在M处,则铁做原电池的正极,这种电化学防护法为牺牲阳极的阴极保护法; 铁为原电池的正极,发生吸氧腐蚀,电极反应为:O2+2H2O+4e—=4OH—。
2OH-+H2↑+Cl2↑。②X为锌,开关在M处,则铁做原电池的正极,这种电化学防护法为牺牲阳极的阴极保护法; 铁为原电池的正极,发生吸氧腐蚀,电极反应为:O2+2H2O+4e—=4OH—。
考点:化学反应与能量
本题难度:困难
2、简答题 甲醇是一种燃料,也可以作为燃料电池的原料.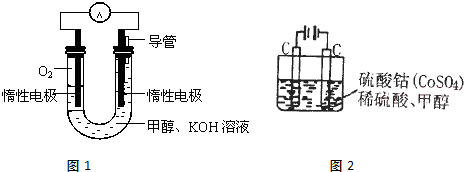
(1)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H1=-1275.6KJ/mol
②2CO?(g)+O2(g)=2CO2(g)△H2=-566.0KJ/mol
③H2O(g)=H2O(l)△H3=-44.0KJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:______;
(2)甲醇直接燃烧会产生一定的污染,某实验小组依据甲醇燃烧的反应原理,设计如图1所示的电池装置,则电池正极的电极反应式:______,该电池工作时,溶液中的OH-向______极移动,该电池工作一段时间后,测得溶液的pH减小,则该电池总反应的离子方程式为______;
(3)甲醇对水质会造成一定的污染,用如图2所示的电化学法可消除这种污染,原理是:通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂再把水中的甲醇氧化成CO2而净化.则用该装置净化含10mol甲醇的水,转移电子数为______.
参考答案:(1)已知:①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1275.6kJ/mol
②2CO?(g)+O2(g)=2CO2(g)△H=-566.0kJ/mol
③H2O(g)=H2O(l)△H=-44.0kJ/mol
利用盖斯定律将①-②2+③可得:CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-442.8kJ/mol,
故答案为:CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-442.8kJ/mol;
(2)碱性甲醇燃料电池中,负极发生氧化反应,电极反应式为CH3OH-6e-+8OH-+=CO32-+6H2O,正极发生还原反应,电极反应式为O2+2H2O+4e-=4OH-,该电池工作时,溶液中的OH-向负极移动,则总反应式为2CH3OH+3O2+4OH-=2CO32-+6H2O,
故答案为:O2+2H2O+4e-=4OH-;负;2CH3OH+3O2+4OH-=2CO32-+6H2O;
(3)甲醇氧化成CO2,C元素的化合价升高+6价,则10mol甲醇失去60mol电子,转移的电子数为60NA,故答案为:60NA.
本题解析:
本题难度:一般
3、选择题 下列依据热化学方程式得出的结论正确的是( )
A.已知2H2(g)+O2(g)═2H2O(g)△H=-483.6?kJ?mol-1说明2?mol?H2(g)和1?mol?O2(g)的能量总和小于2?mol?H2O(g)的能量
B.已知C(s,石墨)═C(s,金刚石)△H>0,则金刚石比石墨稳定
C.已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.4?kJ?mol-1,则含20?g?NaOH的稀溶液与稀盐酸完全中和,放出28.7?kJ的热量
D.已知2C(s)+2O2(g)═2CO2(g)△H12C(s)+O2(g)═2CO(g)△H2,则△H1>△H2
参考答案:C
本题解析:
本题难度:一般
4、填空题 工业制硝酸的主要反应为:4NH3(g)+5O2(g)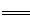 4NO(g)+6 H2O(g)△H。
4NO(g)+6 H2O(g)△H。
(1)已知氢气的燃烧热为285.8 kJ/mol。
N2(g)+3H2(g)=2NH3(g) △H=-92.4 kJ/mol;
H2O(1)=H2O(g)△H=+44.0 kJ/mol;
N2(g)+O2(g)=2NO(g)△H=+180.6 kJ/mol。
则上述工业制硝酸的主要反应的△H= 。
(2)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表: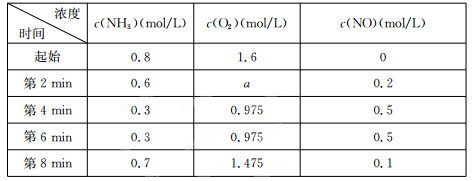
①反应在第2 min到第4 min时,O2的平均反应速率为 。
②反应在第6 min时改变了条件,改变的条件可能是 (填序号)。
A.使用催化剂 B.升高温度 C.减小压强 D.增加O2的浓度
③下列说法中能说明4NH3(g)+5O2(g) 4NO(g)+6 H2 O(g)达到平衡状态的是 (填序号)。
4NO(g)+6 H2 O(g)达到平衡状态的是 (填序号)。
A.单位时间内生成n mol NO的向时,生成n mol NH3
B.条件一定,混合气体的平均相对分子质量不再变化
C.百分含量w(NH3)=w(NO)
D.反应速率v(NH3):u(O2):v(NO):v(H2O)=4:5:4:6
E.若在恒温恒压下容积可变的容器中反应,混合气体的密度不再变化
(3)某研究所组装的CH3OH-O2燃料电池的工作原理如图所示。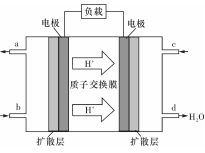
①该电池工作时,b口通入的物质为____ 。
②该电池正极的电极反应式为: 。
③以此电池作电源,在实验室中模拟铝制品表面“钝化”处理(装置如图所示)的过程中,发现溶液逐渐变浑浊并有气泡产生,其原因可能是 (用相关的离子方程式表示)。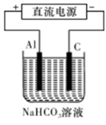
参考答案:(1)-904.8kJ·mol-1 (2)①0.1875mol/(L·min) ②B ③ ABE
(3)①CH3OH ②O2+4e-+4H+=2H2O ③Al3++3HCO3-=Al(OH)3+3CO2(Al-3e-+3HCO3-Al(OH)3+3CO2也给分)
本题解析:(1)H2(g)+1/2O2(g)
本题难度:困难
5、选择题 已知乙硼烷气体(B2H6)在氧气中能剧烈燃烧生成三氧化二硼和水,且生成1mol气态水可放出678 kJ的热量,已知:H2O(l)=H2O(g) △H=44 kJ/mol。下列热化学方程式错误的是
[? ]
A. B2H6(g) +3O2(g)=B2O3(s)+3H2O(l) △H=-2 166kJ/mol
B. B2H6(g)+3O2(g)=B2O3(s)+3H2O(g) △H=-2034kJ/mol
C. B2H6(g)+3O2(g)=B2O3(s)+3H2O(l) △H=-2 078kJ/mol
D. 1/3B2H6(g)+O2(g)=1/3B2O3(s)+H2O(l) △H=-722kJ/mol
参考答案:A
本题解析:
本题难度:简单