时间:2018-03-17 06:57:48
1、选择题 下列叙述正确的是
A.pH为3的盐酸中,其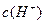 是pH为1的盐酸中的3倍
是pH为1的盐酸中的3倍
B.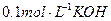 溶液和
溶液和 氨水中,其
氨水中,其 相等
相等
C.在25℃时,无论是酸性、碱性还是中性溶液中,其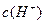 和
和 的乘积都等于
的乘积都等于
D.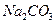 溶液加水稀释后,恢复至原温度,pH和Kw均减小
溶液加水稀释后,恢复至原温度,pH和Kw均减小
参考答案:C
本题解析:略
本题难度:简单
2、选择题 下列说法中正确的是( )
A.在Na3PO4溶液中,c(Na+)是c(PO43-)的3倍
B.pH为3的盐酸中,其c(H+)是pH为1的盐酸中c(H+)的3倍
C.0.1 mol・L-1KOH溶液和0.1 mol・L-1氨水中,其c(OH-)相等
D.在25℃时,无论是酸性、碱性还是中性的稀溶液中,其c(H+)和c(OH-)的乘积都等于1×10-14
参考答案:D
本题解析:A.PO43-水解,c(Na+)>3c(PO43-);B.pH为3的盐酸中c(H+)=10-3mol・L-1,而pH=1的盐酸中c(H+)=10-1 mol・I-1,前者是后者的;C.氨水为弱电解质,部分电离;D.水的离子积适用于纯水和稀的电解质水溶液。25℃时其值为1×10-14。
本题难度:一般
3、选择题
A.0.2 mol/L的NaHCO3溶液:
c(HCO3-)>c(CO32-)>0.1 mol/L>c(H2CO3)
B.pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合:
c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
C.0.2 mol/L CH3COOH溶液和0.2 mol/L CH3COONa溶液等体积混合:
c(CH3COO-)+c(OH-)-c(H+)=0.1 mol/L
D.0.1mol/LNa2CO3溶液与0.1mol/LNaHCO3溶液等体积混合
c(CO32-)+2c(OH-)=?c(HCO3-)+3c(H2CO3)+2c(H+)
参考答案:CD
本题解析:该题要求要求学生根据溶液中盐的水解、弱电解质的电离、电荷守恒等化学变化的规律,判断溶液中离子浓度的相对大小,综合考查学生对电解质溶液基本原理的理解情况和综合分析解决问题的能力。
A中HCO3-、CO32-的浓度不可能都大于0.1 mol/L,否则加起来就大于0.2 mol/L;B中所得混合溶液应显酸性;C实际考查的是电荷守恒,c(Na+)=0.1 mol/L;D中可得电荷守恒等式c(Na+)+c(H+)=?c(HCO3-)+2 c(CO32-)+c(OH-)和物料守恒等式2c(Na+)=3[c(CO32-)+c(HCO3-)+c(H2CO3)],两式消去c(Na+)即可判断。
本题难度:一般
4、选择题 下列过程或现象与 盐类水解无关的是(?)
盐类水解无关的是(?)
A.纯碱溶液去油污

B.草木灰与铵态氮肥不能同时施用
C.使用漂白粉给自来水杀菌
D.浓硫化钠溶液有臭味
参考答案:C
本题解析:略
本题难度:简单
5、填空题 常温下某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合溶液的pH如下表:
| 实验编号 | HA的浓度(mol・L-1) | NaOH的浓度(mol・L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | c | 0.2 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=9 |
参考答案:(1)若a=7,HA为强酸,若a>7,HA为弱酸
(2)否 c(A-)=c(Na+)
(3)弱c(Na+)>c(A-)>c(OH-)>c(H+)
(4)10-5
本题解析:甲实验中酸和碱恰好完全反应生成NaA盐溶液,若a=7,HA为强酸,若a>7,HA为弱酸。乙实验中如果HA为强酸,c=0.2 mol・L-1,若HA为弱酸,c>0.2 mol・L-1。pH=7说明溶液显中性,c(H+)=c(OH-),由电荷守恒可知,c(A-)=c(Na+)。丙组实验时HA过量的情况下混合液显碱性说明HA为弱酸。混合溶液中c(H+)<c(OH-),溶液中离子浓度大小为c(Na+)>c(A-)>c(OH-)>c(H+)。常温下KW=10-14,所以当混合溶液的pH=9时,由水电离的 。
。
本题难度:简单