时间:2018-03-17 06:57:02
1、选择题 25℃时,有浓度均为1 mol/L的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2三种溶液,若测得其中c(NH )分别为
)分别为
参考答案:
本题解析:
本题难度:一般
2、填空题 某盐或“类盐”的化学式为XmYn最简结构,将一定量的该盐溶于足量的水时:
(1)若m≠n,测得溶液的pH为5,则该盐与水反应的离子方程式可能为__________________。
(2)若m≠n,测得该盐溶液的pH为9,则该盐与水反应的离子方程式可能为__________________。
(3)若m≠n,X、Y为同周期的短周期元素,XmYn溶于水时,既有白色沉淀,又有无色气体放出,则溶于水的化学方程式为__________________。
(4)若m≠n,X、Y为不同周期的短周期元素,XmYn溶于水时,既有白色沉淀,又有无色气体放出,则溶于水的化学程式为。__________________。
(5)若X、Y为同主族元素,且m=n,则该物质溶于水的化学方程式为__________________。溶于水后溶液呈碱性,如__________________;溶于水后溶液呈酸性,如__________________。
参考答案:
(1)Xn++nH2O X(OH)n+nH+
X(OH)n+nH+
(2)Ym-+H2O HY(m-1)-+OH-
HY(m-1)-+OH-
(3)Al2S3+6H2O=2Al(OH)3↓+3H2S↑
(4)Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑ ,Al4C3+12H2O=4Al(OH)3↓+3CH4↑
(5)NaH+H2O=NaOH+H2↑,KH+H2O=KOH+H2↑,BrCl+H2O=HBrO+HCl,
IBr+H2O=HIO+HBr ;NaH、KH;BrCl、IBr
本题解析:
本题难度:一般
3、选择题 下列关于离子的叙述正确的是
A.在c(H+)=1×10-13mol・L-1的溶液中:Na+、Fe3+、Cl-、SO42-能大量共存
B.铜溶于FeCl3溶液中:Cu + Fe3+ = Fe2+ + Cu2+
C.NaHCO3溶液中:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
D.向溶液中加入BaCl2溶液后再加盐酸,有白色沉淀,说明该溶液中一定含有SO42-
参考答案:C
本题解析:A、在c(H+)=1×10-13mol・L-1的溶液中:Fe3+不能大量共存,错误;B、铜溶于FeCl3溶液中,离子方程式为Cu+2Fe3+=2Fe2++Cu2+,错误;C、根据物料守恒可知NaHCO3溶液中:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3),正确;D、向溶液中加入BaCl2溶液后再加盐酸,有白色沉淀,说明该溶液中可能含有SO42-,也可能含有Ag+,错误;故本题选择C。
考点:离子的共存,离子方程式的书写,离子浓度的比较,离子的检验
本题难度:一般
4、选择题 下列说法正确的是
A.室温下,pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH)>c(OH-)=c(H+)
B.醋酸与醋酸钠的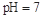 的混合溶液中:c(CH3COO-) + c(CH3COOH)<c(Na+)
的混合溶液中:c(CH3COO-) + c(CH3COOH)<c(Na+)
C.相同物质的量浓度的NaClO和NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-)
D.c(NH4+)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中:c(NH4HSO4) > c[(NH4)2SO4]> c(NH4Cl)
参考答案:C
本题解析:A.氨水是弱碱,PH=11的氨水中,氨水的浓度大于10-3mol/L,盐酸是强酸,PH=3的盐酸溶液,HCl的浓度等于10-3mol/L,等体积混合后,氨水有剩余,溶液显碱性,c(OH-)>c(H+),A项错误;B.根据电荷守恒,醋酸与醋酸钠的PH=7的混合溶液中,c(CH3COO-)=c(Na+),B项错误;C.根据物料守恒,在NaClO溶液中,c(Na+)= c(HClO)+c(ClO-),在NaHCO3溶液中,c(Na+)= c(HCO3-)+c(H2CO3)+c(CO32-),所以c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-),C项正确;D.含有同等浓度的铵根离子的盐中,化学式中含有铵根离子个数越多其浓度越小,硫酸氢铵电离出氢离子抑制铵根离子水解,所以c(NH4+)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中:c[(NH4)2SO4]<c(NH4HSO4)<c(NH4Cl),D项错误;选C。
考点:考查电解质溶液中离子浓度的大小比较。
本题难度:困难
5、选择题 实验测得常温下0.1 mol/L某一元酸(HA)溶液的pH不等于l,0.1 mol/L某一元碱(BOH)溶液里:C(H+)/C(OH―)=10―12。将这两种溶液等体积混合后,所得溶液里各离子的物质的量浓度的关系正确的是
A.C(B+)>C(A―)>C(OH―)>C(H+)?
B.C(A―)>C(B+)>C(H+)>C(OH―)
C.C(B+)+C (H+)=C(A―)+C(OH―)?
D.C(B+)>C(A―)>C(H+)>c(OH―)
参考答案:AC
本题解析:由常温下0.1 mol/L某一元酸(HA)溶液的pH不等于l可知HA为弱酸,又0.1 mol/L某一元碱(BOH)溶液里:C(H+)/C(OH―)=10―12可得BOH为一元强碱;当两者等体积混合后恰好完全反应生成BA溶液,则溶液里各离子物质的量浓度的关系为:C(B+)>C(A―)>C(OH―)>C(H+);又根据电荷守恒得C(B+)+C (H+)=C(A―)+C(OH―)
本题难度:简单