ʱ��:2018-03-17 06:45:10
1������� �û���Ӧ��ͨʽ�ɱ�ʾΪ��
���ʼס��Һͻ�����A��BΪ��ѧ�������ʣ���ش��������⣺
��1�����ʼ�����������;��㷺�Ľ���������������������壬д�����ӷ���ʽ��?��
��2����������A�����³�Һ̬��������B����ɫ��Ӧ�ʻ�ɫ����÷�Ӧ�Ļ�ѧ����ʽΪ?��
��3��������һ�ֺ�ɫ�������ʣ�������B����Һ��dz��ɫ����÷�Ӧ�����ӷ���ʽΪ?��
��4����ҵ�������û���Ӧԭ���Ʊ�һ�ְ뵼����ϣ�д���÷�Ӧ�Ļ�ѧ����ʽ?��
��5�����������Ǻ�ɫ�ǽ������嵥�ʣ�������B��һ�ְ�ɫ�����������÷�Ӧ�Ļ�ѧ����ʽ?��
��6����������BΪ��ɫ���Ծ��壬�����嵥�������ڿ�����ȼ�գ�д���÷�Ӧ�Ļ�ѧ����ʽ?��
�ο��𰸣���1��Fe+2H+=Fe2++H2�� ��2��2Na+2H2O=2NaOH+H2?��3��Fe+Cu2+=Fe2++Cu?
��4��SiO2+2C ?Si+2CO��?��5��2Mg+CO2
?Si+2CO��?��5��2Mg+CO2 2MgO+C?
2MgO+C?
��6��3Fe+4H2O(g) ?Fe3O4+4H2
?Fe3O4+4H2
��������������������������ʵ����ԣ���;������д��ȷ�Ļ�ѧ����ʽ��
�����Ѷȣ�һ��
2������� ��10�֡��ס��ҡ�����������������Һ���ֱ��� ��K+��Al3+��Ag+��Ba2+��Cl-��Br-��
��K+��Al3+��Ag+��Ba2+��Cl-��Br-��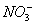 ��
��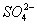 ��
��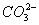 �е�һ�����(���Ӳ��ظ�����)�����мס�������������Һ�����ԣ�����Һ�ʼ��ԣ����ҷ�Ӧ�����ɰ�ɫ���������壬���ɷֱ���ס��ҡ�����Ӧ���ɰ�ɫ����������������ʵ�ƶ�������Һ�����ʵĻ�ѧʽ��
�е�һ�����(���Ӳ��ظ�����)�����мס�������������Һ�����ԣ�����Һ�ʼ��ԣ����ҷ�Ӧ�����ɰ�ɫ���������壬���ɷֱ���ס��ҡ�����Ӧ���ɰ�ɫ����������������ʵ�ƶ�������Һ�����ʵĻ�ѧʽ��
��___________����___________����___________����___________����___________��
�ο��𰸣��ף�Al2(SO4)3?�ң�K2CO3?����AgNO3?����BaCl2?�죺NH4Br
����������ס�������������Һ�����ԣ����ж�ʱ����H+������Һ�Լ��ԣ����ж�ʱ����OH-��Ȼ��������Ӽ�ķ�Ӧ�������ƶϡ�
�����Ѷȣ���
3���ƶ��� ��֪A����;��㷺�Ľ������ʣ�B�dz����³�Һ̬�Ļ����E��һ�ֻ���ɫ�����塣��ͼ�в��ֲ���δ�������?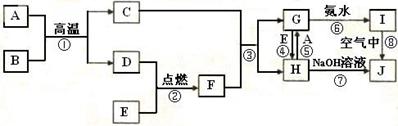
�ش��������⣺
(1)д��C�Ļ�ѧʽ?��д����Ӧ�ٵĻ�ѧ��Ӧ����ʽ��?��
(2)д����Ӧ�۵����ӷ���ʽ?
д����Ӧ�ܵ����ӷ���ʽ________________________________________
(3)����G��Һ�������ӵķ��� ?��
(4)��H��Һ�μӵ���ˮ�У�����������У��õ�����Һ��ɫΪ_________
��ɢ�ʵĴ�С��___________________.
�ο��𰸣���ÿ�ո�2�֣���14�֣���1��Fe3O4? 3Fe��4H2O(g)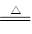 Fe3O4��4H2��
Fe3O4��4H2��
(2)F3O4��8H��=2Fe3����Fe2����4H2O? 2Fe2����Cl2=2Fe3��2Cl��
(3)�ȼ����軯����Һ��û�������ټ���ˮ����Һ��졣��Ҳ��д������������Һ��
(4)���ɫ? 1nm----100nm
���������A����;��㷺�Ľ������ʣ���A������B�dz����³�Һ̬�Ļ�������ڸ������ܺ�����Ӧ������B��ˮ��E��һ�ֻ���ɫ�����壬��E�����������ڸ����º�ˮ������Ӧ��������������������������D�������ɷ�Ӧ����˵��D��������C��������������F���Ȼ��⣬����ˮ���õ����ᡣ�����������������Ӧ�����Ȼ������Ȼ�������H�ܺ�����Ӧ����G������H���Ȼ�����G���Ȼ���������I��������������J������������
�����������Ǹ߿��еij������ͣ����ڻ���������Ŀ��顣�����������У�����֪ʶ�����ض�ѧ������֪ʶ�Ĺ��̸�ѵ��������������Ҫע����ǻ�ѧ�ƶ�����һ���ۺ��Խ�ǿ�����⣬��Ԫ�ؼ����������ʺ�������������������ѧ�����֪ʶ����������ѧ�Ƽ��ۺϡ��������ɿ���ѧ���Ի�ѧ֪ʶ������̶ȣ�����Ҫ��������ѧ�����ۺϷ���������˼ά���������ͼ��ķ�������ؼ�����Ѱ�ҡ�ͻ�ƿڡ�����ͻ�ƿڡ�����ץ���ء��֣�����������ɫ������״̬��������ζ�����ⷴӦ���������������Ʒ���������;�ȡ�
�����Ѷȣ�һ��
4���ƶ��� ����A��G����ͼ��ʾת����ϵ(���ַ�Ӧ�������û���г�)������AΪij���������Ҫ�ɷ֣�����һϵ�з�Ӧ�ɵõ�B��C.����C����E��Ũ��Һ������Ӧ��GΪש��ɫ������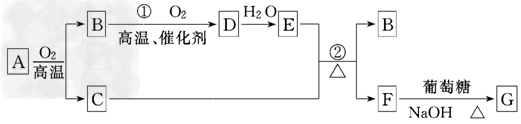
��ش��������⣺
(1)д���������ʵĻ�ѧʽ��B________��E__________��G________��
(2)���õ����ᴿC���ʣ��ڸõ�ⷴӦ������������________������������________���������Һ��________��
(3)��Ӧ�ڵĻ�ѧ����ʽ��_______________________��
�ο��𰸣�(1)SO2��H2SO4��Cu2O
(2)��ͭ����ͭ��CuSO4��Һ
(3)Cu��2H2SO4(Ũ) CuSO4��SO2����2H2O
CuSO4��SO2����2H2O
���������
�����Ѷȣ�һ��
5������� ��ij��ɫ����A���������ȣ�Ͷ�뵽��һ����ɫŨ��ҺB�У�����������������ɵĻ������X����X����ͼ��ʾ��ʵ�飺
����д���пհף�
��д��A��B��Ӧ�Ļ�ѧ����ʽ______��
����ɫ����C�ijɷ�Ϊ______��
��д��D��F��Ӧ�����ӷ���ʽ______��
������Na2CO3Ϊԭ�ϣ����һ����ʵ��֤��D��F��Ӧ���ɵ�����E����ɫ�ģ�����ʵ�����______��
�ο��𰸣���ɫ����Cͨ�����ʯ��ˮ���ɰ�ɫ�������ó���ӦΪCaCO3��˵��C�к���CO2����ɫϡ��ҺD�뵥��F��Ӧ������ɫ��Һ������ҺӦ����Cu2+����˵��FΪCu����ɫϡ��ҺD����ǿ�����ԣ�ӦΪϡHNO3��Һ����������EΪNO����˵���������XӦΪCO2��NO2�Ļ�����AΪC��BΪHNO3����
��A��BΪC��Ũ����ķ�Ӧ����Ӧ�ķ���ʽΪC+4HNO3��Ũ��?��?.?CO2��+4NO2��+2H2O��
�ʴ�Ϊ��C+4HNO3��Ũ��?��?.?CO2��+4NO2��+2H2O��
�������Ϸ�����֪��ɫ����C�ijɷ�ΪCO2��NO���ʴ�Ϊ��CO2��NO��
��ϡ�����Cu��Ӧ�����ӷ���ʽΪ3Cu+2NO3-+8H+�T3Cu2++2NO��+4H2O��
�ʴ�Ϊ��3Cu+2NO3-+8H+�T3Cu2++2NO��+4H2O��
��D��F���ɵ�����ΪNO�����������������Ӧ���ɺ���ɫ��NO2��Ϊ�ų�������Ӱ�죬Ӧ������Na2CO3��ĩ��Ȼ��������ϡHNO3�������ɵ�CO2���Թ��ϲ�������ȫ�ž����ټ���Cu���ȣ����ɹ۲쵽����ɫ����NO���ɣ�
�ʴ�Ϊ��ȡһ֧�Թܣ�������Na2CO3��ĩ��Ȼ��������ϡHNO3�������ɵ�CO2���Թ��ϲ�������ȫ�ž����ټ���Cu���ȣ����ɹ۲쵽����ɫ����NO���ɣ�
���������
�����Ѷȣ�һ��