ʱ��:2018-03-17 06:16:23
1��ѡ���� ���ſ�ѧ�����IJ��Ͻ������о����ʵ��ֶκ�;��Խ��Խ�࣬������Ӽ�������Ƭ��C60��N5+��H3��
O4������̱����֡������й���Щ���ʵ�˵���У���ȷ����
[? ]
A��N5+�������36������
B��C60��Ħ������Ϊ720g
C��H2��H3����ͬ��������
D��O2��O4����ͬλ��
�ο��𰸣�C
���������
�����Ѷȣ���
2��ѡ���� ij���Ӻ���6�����ӣ�7�����ӣ����Ϊ0�������Ļ�ѧ������
A.136Al
B.136Al
C.13 6 C
D.136C
�ο��𰸣�C
��������������������·�Ϊ6��̼��������=������+������=13�������Ϸ���C��ȷ��
�����Ѷȣ�һ��
3������� �������һ���ױ�ѹ����Һ�������壬Һ�����ڹ���ѭ��������ʱ����������ʹ�����¶Ƚ��ͣ��ﵽ����Ŀ�ġ����������ù����ѡ�NH3��CH3Cl����������������Dz����ж���������ȼ�����ǿ�ѧ�Ҹ���Ԫ�����ʵĵݱ� �����������µ����������������֪ʶ��ijЩԪ�ػ��������ȼ�ԡ����Ա仯�������£�
(1)�⻯�����ȼ�ԣ��ڶ����ڣ�____>____>H2O>HF���������ڣ�SiH4>PH3>____>____��
(2)������Ķ��ԣ�PH3>NH3��H2S____H2O��CS2____CO2��CCl4_____CF4���>������<����=���������ǿ�ѧ���ǿ�ʼ��ע���������ں�F��Cl�Ļ������ϡ�
(3)��֪CCl4�ķе�Ϊ76.8��C��CF4�ķе�Ϊ-128�棬��������ķе㷶ΧӦ������䡣�����ϳ�ʱ�䷴�� ���飬һ���µ������������CF2Cl2���ڵ����ˣ��������ƵĻ�������_____________________��
(4)Ȼ�����������������˵����ijһ����������___________����������Ԫ�����ڱ���Ԫ�ؼ��仯�����________����д��ĸ���仯����������������Ŀ�ѧ˼ά������ֵ�ý���ġ�
�ٶ��� �ڷе� ����ȼ�� ��ˮ���� ����ɫ
a.�٢ڢ� b.�ڢܢ� c.�ڢۢ�
�ο��𰸣�(1)CH4��NH3��H2S��HCl
(2)>��>��>
(3)CFCl3(��CF3Cl)
(4)ʹ������������ֿն���a
���������
�����Ѷȣ�һ��
4������� �����������ݵĹ��ɽ�������
��1��ͬ��Ԫ�ص��ʼ���û���Ӧ�Ļ�ѧ����ʽ��
��2Na+2H2O=2NaOH+H2��?��2HBr+Cl2=2HCl+Br2 ��2H2S+O2=2S+2H2O?��______
�� 91ExAM.org2����֪
| ��ѧ�� | Si-O | Si-Cl | H-Cl | Si-Si ����/KJ?mol-1 460 360 431 176 |
| 1 2 |
| 1 2 |
�ο��𰸣���1���ڢ�A��Ԫ��C��ǿ��ԭ�ԣ������ܺͶ������跢���û���Ӧ�����ɹ��һ����̼���ʴ�Ϊ��SiO2+2C?����?.?Si+2CO��
��2���ٻ�ѧ���ļ���Խ���ƻ���ѧ�����������Խ�����ʵ��۵�Խ�ߣ���ͼ��֪��Si-O���ļ��ܱ�Si-Cl���ļ��ܴ�����SiCl4���۵��SiO2���۵�ͣ�
�ʴ�Ϊ������
��12SiCl4��g��+H2��g��=12Si��s��+2HCl��g����H=+118 KJ?mol-1��
��H=��Ӧ��ļ���-������ļ���=��12��360��4+H-H�ļ���-12��176��2-2��431��KJ?mol-1=+118 KJ?mol-1
H-H����Ϊ436 KJ?mol-1���ʴ�Ϊ��436��
���������
�����Ѷȣ�һ��
5������� I�����ǵؿ��к�����ߵĽ���Ԫ�أ��䵥�ʼ���Ͻ������������е�Ӧ��ʮ�ֹ㷺��
(1)����������������Al2O3Ϊԭ�ϣ������ʯ(Na3AlF6)������״̬�½��е�⣬��ѧ����ʽΪ��??����缫����ʯī�������ɣ�����ʱ�������ĵĵ缫��?��(���������������)��
(2)������Ʒ���п���ʴ���������ӳ���ʹ���������Դ�����������Ϊ��������H2SO4��Һ�е�⣬���ı����γ�����Ĥ��������ӦʽΪ?��
(3)�����������Խ��Al-Ag2O��ؿ�����ˮ�¶�����Դ����ѧ��ӦΪ2Al+3Ag2O+2NaOH+3H2O�T2Na[Al(OH)4]+6Ag�����ĵ缫��ӦʽΪ?������������Һ��pH?(��������С)��
II�����ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���á�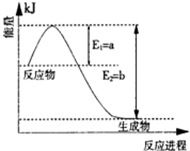
(1)ͼ����һ���¶Ⱥ�ѹǿ��N2��H2��Ӧ����1molNH3�����������仯ʾ��ͼ����д���ϳɰ����Ȼ�ѧ��Ӧ���̣�?(��H����ֵ�ú���ĸa��b�Ĵ���ʽ��ʾ)��
(2)��ҵ�ϳɰ���Ӧ���£�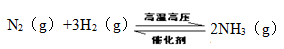
��һ���¶��£���һ������N2��H2ͨ�뵽���Ϊ1L���ܱ������У���Ӧ�ﵽƽ��ı�������������ʹƽ��������Ӧ�����ƶ���ƽ�ⳣ���������?��
A������ѹǿ
B������Ӧ���Ũ��
C��ʹ�ô���
D�������¶�
�������仯����������������й㷺Ӧ�ã���ش��������⣺
(1)������(FeS2)�����������ұ����������Ҫԭ�ϣ�����һ����ӦΪ��
��3mol?FeS2�μӷ�Ӧ��ת��?mol���ӡ�
(2)�Ȼ�����Һ��Ϊ��ѧ�Լ��еġ������֡���д��SO2ͨ���Ȼ�����Һ�з�Ӧ�����ӷ���ʽ?��
�ο��𰸣���.(1)2Al2O3=2Al+3O2������
(2)2Al+3H2O-6e-=Al2O3+6H+
(3)Al-3e-+4OH-=AlO2-+H2O?���
��.(1)N2(g)+3H2(g)=2NH3(g)��H=-2(b-a)kJ/mol
(2)AB
��(1)32
(2) 2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
���������I��(1)��Al2O3Ϊԭ�ϣ������ʯ(Na3AlF6)������״̬�½��е����������������Ӧ�Ļ�ѧ����ʽΪ��2Al2O3=2Al+3O2�������������������ĵ缫ʯī��
(2)������Ʒ���п���ʴ���������ӳ���ʹ���������Դ�����������Ϊ��������H2SO4��Һ�е�⣬�������γ�����Ĥ����ʧ������������������Ӧ�������缫��ӦΪ��2Al+3H2O-6e-=Al2O3+6H+��
(3)��ѧ��ӦΪ2Al+3Ag2O+2NaOH+3H2O�T2Na[Al(OH)4]+6Ag����������ʧ�����ڼ���Һ���������ǻ��������ƣ����ĵ缫��Ӧʽ��Al+4OH--3e-=[Al(OH)4-]����Al-3e-+4OH-=AlO2-+2H2O
II��(1)ϸ�Ĺ۲�ͼ��֪��N2��H2��Ӧ����1molNH3�ų�������Ϊ(b-a)kJ���÷�Ӧ���Ȼ�ѧ��Ӧ����ʽΪN2(g)+3H2(g)==2NH3(g)��H=-2(b-a)kJ?mol-1
(2)һ���¶��£���һ������N2��H2ͨ�뵽���Ϊ1L���ܱ������У���Ӧ�ﵽƽ��ı�������������ʹƽ��������Ӧ�����ƶ���ƽ�ⳣ�����䣬��������ѹǿ��ƽ��������У���ƽ�ⳣ�����䣬��A��ȷ������Ӧ���Ũ�ȣ�ƽ��������У�ƽ�ⳣ�����䣬��B��ȷ��ʹ�ô������ܸı�ƽ�⣬ƽ�ⲻ����ƽ�ⳣ��Ҳ���䣬��C������������Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ������ȷ�Ӧ������У���ƽ��������У�ƽ�ⳣ�����ʴ���
III(1) ����3mol FeS2�μӷ�Ӧ������ת��Ϊ8��2��2=32mol���ʴ�Ϊ��32
����3mol FeS2�μӷ�Ӧ������ת��Ϊ8��2��2=32mol���ʴ�Ϊ��32
(2)��������ͨ���Ȼ�����Һ�з�����Ӧ��������������Ϊ���ᣬ�Ȼ�������ԭΪ�Ȼ���������Ӧ�����ӷ���ʽΪ��2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
�����Ѷȣ�һ��