ʱ��:2018-03-17 05:54:38
1��ѡ���� ��֪��Ӧ����101 kPaʱ��2H2(g)+O2(g) ==2H2O(g)?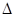 H="-483.6" kJ/mol
H="-483.6" kJ/mol
��ϡ��Һ�У�H+(aq)+OH-(aq)==H2O(l)?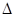 H="-57.3" kJ/mol
H="-57.3" kJ/mol
��֪��H2��O2�������巴Ӧ����1 molҺ̬ˮ������1mol��̬ˮ��ų�44kJ���������н�������ȷ���ǣ�?��
A��H2��ȼ����Ϊ285.8 kJ/mol
B��H2��O2��Ӧ����Һ̬ˮʱ���Ȼ�ѧ����ʽΪH2(g) +1/2O2(g)=H2O(l)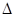 H="-571.6" kJ/mol
H="-571.6" kJ/mol
C��ϡ������ϡNaOH��Һ��Ӧ���к���Ϊ-57.3 kJ
D��ϡ������ϡNaOH��Һ��Ӧ����1molˮ���ų�57.3kJ����
�ο��𰸣�A
���������������֪��H2O(g)= H2O(l) 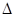 H="-44" kJ/mol��
H="-44" kJ/mol��
2H2(g)+O2(g) ==2H2O(g)?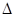 H="-483.6" kJ/mol
H="-483.6" kJ/mol
��ʽ��ӿ��Ƶã�2H2(g) +O2(g)=2H2O(l)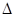 H="-571.6" kJ/mol
H="-571.6" kJ/mol
����ȼ���ȸ����֪H2��ȼ����Ϊ285.8 kJ/mol������A��ȷ��B����ȷ��
C���к��ȵĵ�λ��kJ/mol
D������Ϊ���ᣬ���к����е�����Ҫ���IJ�������������ϡ������ϡNaOH��Һ��Ӧ����1molˮʱ�ų�������С��57.3kJ
�����Ѷȣ�һ��
2�������� (1)25��ʱ����ˮ(D2O)�����ӻ�Ϊ1.6��10-15��Ҳ����pHһ���Ķ������涨�����ȣ�pD=��lgc(D��)��
��д����ˮ�ĵ��뷽��ʽ��
����25��ʱ����ˮ�и������ӵ����ʵ���Ũ�ȣ�
����25��ʱ����ˮ��pD��
��2 ����100mL 2mol/L��Ba(OH)2��Һ�еμ�100mL NaHSO4��Һ�������Һ��pHΪ1��������ij����������Լ�NaHSO4��Һ�����ʵ���Ũ�ȡ�
����100mL 2mol/L��Ba(OH)2��Һ�еμ�100mL NaHSO4��Һ�������Һ��pHΪ1��������ij����������Լ�NaHSO4��Һ�����ʵ���Ũ�ȡ�
�ο��𰸣�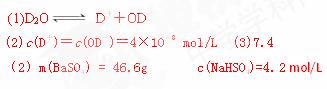
�����������
�����Ѷȣ�һ��
3������� ��7�֣�
��1����25�������½�pH=11�İ�ˮϡ��100������Һ��pHΪ?������ţ���
A��9
B��13
C��11��13֮��
D��9��11֮��
��2��pH=3�Ĵ����pH=11������������Һ�������Ϻ����Һ��c��Na����
?c��CH3COO�������>������=����<������
��3�������£���֪ijNH4Cl��Һ�е�c��NH4����=c��Clһ���������Һ��pH?7���>������=����<������
��4�������HCl��CH3COONa��Һ��Ũ�ȡ��������ϣ�������Һ�и�����Ũ�ȵĴ�С��ϵΪ?
�ο��𰸣�
��1��D ��1�֣�?��2��< ��2�֣�?��3�� ="?" ��2�֣�
��4�� c��Cl����=c��Na+��>c��H+��>c��CH3COO����>c��OH������2�֣�
�����������
�����Ѷȣ���
4��ѡ���� δ������Դ���ص�����Դ�ḻ��ʹ��ʱ�Ի�������Ⱦ�������Ⱦ������Щ��������������ȫ����������Դ����һ����
����Ȼ�� ��ú �ۺ��� ��ʯ�� �ݺ����� ������ �߷��� ������
A���٢ڢۢ�
B���ݢޢߢ�
C���ۢܢݢ�
D�����٢���
�ο��𰸣�B
����������١� �� ���� �� �ܾ������������� ���� �� �ܻ�Ի��������Ⱦ�����Բ���������Դ��
���㣺��Դ�뻷�����⡣
�����Ѷȣ���
5��ѡ���� 1mol��ȼ����ȫȼ�������ȶ������������ų�����Ϊȼ���ȣ�����ȼ�շ�Ӧ�ķ�Ӧ�Ȳ���ȼ���ȵ��ǣ�������
��H2��g��+
| 1 2 |
| 1 2 |
�ο��𰸣���H2��g��+12O2��g���TH2O��l����H1������ȼ���ȵĶ��壬����ȷ��
��C��s��+12O2��g���TCO��g����H2�����ɲ��ﲻ���ȶ�������ʴ���
��S��s��+O2��g���TSO2��g����H3������ȼ���ȵĶ��壬����ȷ��
��2H2S��g��+3O2��g���T2SO2��s��+2H2O��l����H4����ȼ������ʵ�������1mol����H4���Բ���ȼ���ȣ��ʴ������Դ�����Ǣڢܣ�
��ѡ��D��
���������
�����Ѷȣ�һ��