时间:2018-03-17 05:24:37
1、选择题 下列各式中属于正确的水解反应的离子方程式的是
[? ]
A. CH3COOH + OH- CH3COO-+H2O
CH3COO-+H2O
B. S2-+2H2O H2S+2OH-?
H2S+2OH-?
C.CH3COOH+H2O CH3COO-+H3O+?
CH3COO-+H3O+?
D.NH4++H2O NH・ H2O+H+?
NH・ H2O+H+?
参考答案:D
本题解析:
本题难度:简单
2、选择题 下列物质加入水中,能使水的电离度增大,溶液的pH值减小的是
A.HCl
B.Al2(SO4)3
C.Na2CO3
D.NH3・H2O
参考答案:B
本题解析:A、加热氯化氢,则溶液的氢离子浓度增大,所以会抑制水的电离,水的电离程度减小,错误;B、铝离子与水电离产生的氢氧根离子结合为氢氧化铝,使水电离产生的氢氧根离子浓度减小,所以会促进水的电离平衡正向移动,水的电离程度增大,氢离子浓度增大,溶液的pH减小,正确;C、碳酸根离子与水电离产生的氢离子结合为碳酸氢根离子,使水电离产生的氢离子浓度减小,水的电离平衡正向移动,但氢氧根离子浓度增大,溶液的pH增大,错误;D、一水合氨是弱碱,加入水中,会抑制水的电离,错误,答案选B。
考点:考查条件对水电离的影响
本题难度:一般
3、填空题 【化学――选修2:化学与技术】(15分)
无水AlCl3易升华,可用作有机合成的催化剂等。工业上由铝土矿(A12O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下。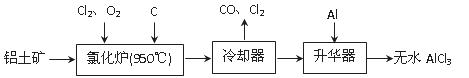
(1)氯化炉中Al2O3、C12和C反应的化学方程式为 。
(2)用Na2SO3溶液可除去冷却器排出尾气中的Cl2,此反应的离子方程式为 。
(3)升华器中主要含有AlCl3和FeCl3,需加入少量Al,其作用是 。
(4)为测定制得的无水AlCl3产品(含杂质FeCl3)的纯度,称取16.25 g无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,残留固体质量为0.32 g。
①写出除杂过程中涉及的离子方程式 、 。
②AlCl3产品的纯度为 。
(5)工业上另一种由铝灰为原料制备无水AlCl3工艺中,最后一步是由AlCl3・6H2O脱水制备无水AlCl3,实现这一步的方法是 。
(6)生铁中含有一种铁碳化合物(Fe3C),工业上要测定碳元素的质量分数,第一步是在足量的空气中煅烧,生成有磁性的固体,该反应的化学方程式是 。
参考答案:(1)Al2O3+3Cl2+3C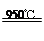 2AlCl3+3CO(2分)
2AlCl3+3CO(2分)
(2)SO32-+Cl2+H2O=SO42-+2Cl-+2H+(2分)
(3)除去FeCl3(2分)
(4)①Fe3++3OH-=Fe(OH)3↓(2分) Al3++4OH-=AlO2-+2H2O(2分)②96%(2分)
(5)在HCl气流中加热脱结晶水(2分)
(6)Fe3C+3O2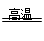 Fe3O4+CO2(1分)
Fe3O4+CO2(1分)
本题解析:⑴在氯化炉中发生的反应物有Al2O3、Cl2、C,生成物有AlCl3、CO(在冷却器中逸出),根据氧化还原反应的配平方法将其配平,并写出反应条件(950℃);
⑵书写Na2SO3溶液与Cl2反应的离子方程式时,先根据得失电子守恒有SO32-+Cl2
本题难度:困难
4、选择题 下列有关电解质的说法中正确的是
A.物质的量相同的磷酸钠溶液和磷酸溶液中所含PO43―的量相同
B.将NaOH和氨水溶液各稀释一倍,两者OH―浓度均减少到原来的1/2
C.强电解质溶液的导电能力不一定比弱电解质溶液强
D.如果盐酸的浓度是醋酸浓度的二倍,则盐酸中c(H+)也是醋酸中c(H+)的二倍
参考答案:C
本题解析:
试题解析:磷酸钠是强电解质,完全电离出钠离子和磷酸根离子,磷酸是弱电解质,微弱电离出磷酸根和氢离子,故A错误;一水合氨是弱电解质,所以氨水中存在电离平衡,氢氧化钠是强电解质,完全电离,所以将NaOH和氨水溶液各稀释一倍 ,氢氧化钠溶液中氢氧根离子浓度是原来的一半,但氨水中氢氧根离子浓度大于原来的一半,故B错误;溶液的导电能力与离子浓度成正比,与电解质的强弱无关,所以强电解质溶液的导电能力不一定比弱电质溶液强,故C正确;醋酸是弱电解质,存在电离平衡,氯化氢是强电解质,在水溶液里完全电离,所以如果盐酸的浓度是醋酸溶液的二倍,则盐酸的H+浓度大于醋酸H+浓度的二倍,故D错误。
考点:弱电解质的电离
本题难度:一般
5、选择题 有① Na2CO3溶液 ② CH3COONa溶液 ③ NaOH溶液各25mL,物质的量浓度相等,下列说法正确的是
A.3种溶液pH的大小顺序是 ③>②>①
B.若分别滴加25mL和上述溶液等浓度的盐酸后,pH最大的是①
C.若将3种溶液稀释相同倍数,pH变化最大的是②
D.若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>②
参考答案:C
本题解析:A.等浓度时强碱的pH最大,强碱弱酸盐中对应的酸性越强,水解程度越小,碳酸的酸性小于醋酸的,所以三种溶液pH的大小顺序是③>①>②,故A错误;B.稀释时强碱的变化程度大,所以三种溶液稀释相同倍数,pH变化最大的是③,故B错误;C.等体积等浓度混合后,①中溶质为NaHCO3、NaCl,②中溶质为NaCl、CH3COOH,③中溶质为NaCl,HCO3-离子水解显碱性,所以pH最大的是①,C正确;D.三种溶液的pH均为9,c(OH-)=10-5mol/L,c(NaOH)=10-5mol/L,但碳酸的酸性小于醋酸的酸性,所以c(Na2CO3)>c(CH3COONa)>10-5mol/L,所以三种溶液的pH均为9,则物质的量浓度的大小顺序是①>②>③,故D错误;故选C.
考点:盐类水解的应用
本题难度:一般