时间:2018-03-17 05:22:50
1、填空题 (10分)实验室有三瓶失去标签的无色溶液:氯化钾、氢氧化钙和稀硫酸,可用一种常见酸碱指示剂X 或Na2CO3一次鉴别它们。根据有关操作及所加试剂填空。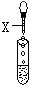 ?
?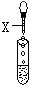 ?
?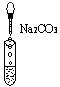
A? B? C
(1)A试管中的现象:溶液显紫色;另取该溶液滴入Na2CO3溶液中,无明显现象。
试推断试剂X为?。
(2)B试管中的现象:溶液显蓝色;另取该溶液滴入Na2CO3溶液中的现象为? ___
有关反应的离子方程式为? __________。
(3)C试管中的现象:有气泡产生,有关反应的离子方程式为? _________;?
另取该溶液滴入试剂X, 则溶液显 _____________。
参考答案:(每空2分,共10分)(1)紫色石蕊试液
(2)有白色沉淀产生;CO32-+Ca2+=CaCO3↓?(3)CO32-+2H+=H2O+CO2↑;红色
本题解析:(1)氯化钾是盐,溶液显中性,氢氧化钙是强碱,硫酸是强酸。根据酸碱指示剂的变色可知,A中溶液显紫色,这说明X一定是紫色的石蕊试液,因此A中的溶液一定不是硫酸。又因为另取该溶液滴入Na2CO3溶液中,无明显现象,所以该溶液是氯化钾。
(2)碱能使紫色的石蕊试液显蓝色,所以B中溶质是氢氧化钙,则滴入Na2CO3溶液中的现象为有白色沉淀生成,反应的离子方程式是CO32-+Ca2+=CaCO3↓。
(3)C中是硫酸。硫酸和碳酸钠反应生成CO2气体,反应的离子方程式CO32-+2H+=H2O+CO2↑;酸能使紫色的石蕊试液显红色。
点评:该题是高考中的常见题型,试题基础性强,难易适中。该题的突破点是溶液显紫色,然后再依据有关物质的化学性质,逐一分析、排除即可得出正确的结论。该题有利于培养稀释的逻辑思维能力和发散思维能力。
本题难度:一般
2、填空题 (4分)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取分液
B.升华
C.结晶
D.分液 E.蒸馏 F.过滤
(1)分离粗盐中混有的泥沙______。?(2)分离碘和水的 混合物______。
混合物______。
(3)分离水和汽油的混合物______。?(4)分离酒精和水的混合物______。
参考答案:F? A? D? E
本题解析:略
本题难度:简单
3、选择题 等物质的量的下列化合物在相应条件下完全分解后,得到的O2最多的是
A.KClO3(加MnO2催化剂,加热)
B.KMnO4(加热)
C.H2O2(水溶液,加MnO2催化剂)
D.HgO(加热)
参考答案:A
本题解析:
本题难度:一般
4、选择题 为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液。不合理的操作顺序是
A.①④②⑤③
B.⑤④②①③
C.②⑤④①③
D.⑤②④①③
参考答案:A
本题解析:根据题意知,粗盐中的杂质离子为钙离子、镁离子、和硫酸根离子,为保证杂质离子除尽,所加试剂要过量,镁离子用加入稍过量的NaOH溶液沉淀,硫酸根离子用稍过量的BaCl2 溶液沉淀,先除镁离子,还是先除硫酸根离子都行;钙离子用稍过量的Na2CO3溶液沉淀,加入的碳酸钠要放在加入的氯化钡之后,碳酸钠会除去反应剩余的钡离子,过滤要放在所有的沉淀操作之后,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,综上所述不正确的选A。
本题难度:一般
5、选择题 下列实验操作中正确的是
[? ]
A.进行蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
B.进行蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的底部
C.进行分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
参考答案:C
本题解析:
本题难度:简单