时间:2017-11-11 04:16:29
1、填空题 (9分)发射卫星时可用肼(N2H4)作燃料,二氧化氮作氧化剂,两者反应生成氮气和水蒸气。已知:N2(g) +2 O2(g) = 2NO2(g);△H=+67.7kJ・mol-1
N2H4(g) + O2(g) = N2(g) + 2H2O(g);△H=-534kJ・mol-1
1/2H2(g) + 1/2F2(g) = HF(g);△H=-269kJ・mol-1
H2(g) + 1/2O2(g) = H2O(g);△H=-242kJ・mol-1
(1)肼和二氧化氮反应的热化学方程式为 ;此反应用于火箭推进,除释放大量能量和快速产生气体外,还有一个很大的优点是:__________ 。
(2)有人认为若用氟气代替二氧化氮作氧化剂,则反应释放的能量更大。肼和氟气反应的热化学方程式为 ___。
参考答案:(1) N2H4(g) + NO2(g) = 3/2 N2(g) + 2H2O(g) △H=-567.9kJ・mol-1
产物为N2和H2O,对环境无污染。
(2) N2H4(g) +2 F2(g) = N2(g) + 4 HF(g);△H=-1126kJ・mol-1
本题解析:(1)考查盖斯定律的应用。根据反应①N2(g) +2 O2(g) = 2NO2(g)和反应②N2H4(g) + O2(g) = N2(g) + 2H2O(g)可知,②-1/2①即得到 N2H4(g) + NO2(g) = 3/2 N2(g) + 2H2O(g),所以反应热是
本题难度:一般
2、填空题 (8分)A、B、C、D四种元素均为元素周期表中的短周期元素,原子序数依次增大,A元素基态原子中p电子数是s电子数的二分之一,B元素最高价氧化物的水化物与其氢化物能够反应生成一种盐,C元素与D元素能形成原子个数比为1:2和1:1的两种常见离子化合物。
(1)A、B、C三种元素的电负性从大到小的顺序是_______________(填元素符号)
(2)D元素原子核外的电子排布式是______________.
(3)B元素与D元素形成的化合物DB2的晶体类型为____________.B2中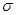 键与
键与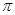 键数目之比为_________________.
键数目之比为_________________.
(4)A、C、D三种元素形成的原子个数比为A:C:D=1:2:1简单化合物的水溶液呈碱性,其原因为(用离子方程式表示):___________________________________________.
(5)已知:B2(g)+2C2(g)=2BC2(g) △H=+67.6kJ・mol-1
B2H4(g)+C2(g)=B2(g)+2H2C(g) △H=-534kJ・mol-1
请写出BC2(g)与B2H4(g)反应生成B2(g)和H2C(g) 的热化学方程式:___________________.
参考答案:(1)O>N>C(1分)(2)1S22S22P63S1(1分)
(3)离子晶体(1分) 1:2(1分)
(4)C2O42-+H2O HC2O4-+OH-(2分)
HC2O4-+OH-(2分)
(5)2NO2(g)+2N2H4(g)==3N2(g)+4H2O(g);△H=-1135.7kJ・mol-1(2分)
或NO2(g)+N2H4(g)==3/2N2(g)+2H2O(g);△H=-567.85kJ・mol-1
本题解析:由题意知A、B、C、D四种元素分别为C、N、O、Na,同周期元素电负性从左至右依次增大;DB3是NaN3,NaN3中N、N之间以共价键结合;N2的三键中有一个δ键,有两个π键;A、C、D三种元素形成的原子个数比为A:C:D=1:2:1简单化合物是Na2C2O4,C2O42-发生水解,水解以第一步为主;(5)利用盖斯定律可得将第二个反应乘以2减去第一个反应即可得到所需反应的热效应。
考点:元素周期表和元素周期律,盐类的水解,热化学方程式
本题难度:困难
3、选择题 已知:N2+O2 2NO?△H=+180 kJ/mol,其中N≡N,O=O键的键能分别是946 kJ/mol、498 kJ/mol,则NO中化学键的键能为
2NO?△H=+180 kJ/mol,其中N≡N,O=O键的键能分别是946 kJ/mol、498 kJ/mol,则NO中化学键的键能为
A.812 kJ/mol
B.632 kJ/mol
C.1264 kJ/mol
D.1624 kJ/mol
参考答案:B
本题解析:旧键断裂吸收的能量减去新键生成释放的能量值即为反应热,据此可以解答。根据N2、O2分子中化学键的键能分别是946kJ?mol-1、498kJ?mol-1以及反应N2+O2 2NO?△H=+180 kJ/mol,可设NO分子中化学键的键能为X,则有:946kJ?mol-1+498kJ?mol-1-2X=180kJ?mol-1,解得X=632kJ?mol-1,所以答案选B。
2NO?△H=+180 kJ/mol,可设NO分子中化学键的键能为X,则有:946kJ?mol-1+498kJ?mol-1-2X=180kJ?mol-1,解得X=632kJ?mol-1,所以答案选B。
本题难度:一般
4、选择题 下列反应的离子方程式书写错误的是
A.铁跟稀硫酸反应:Fe+2H+→Fe2++H2↑
B.醋酸跟氢氧化钾溶液反应:CH3COOH+OH-→CH3COO-+H2O
C.硫化亚铁中加入盐酸:S2-+2H+→H2S↑
D.碳酸钙溶于盐酸中:CaCO3+2H+→Ca2++H2O+CO2↑
参考答案:C
本题解析:分析:A.铁跟稀硫酸反应生成Fe2+和H2;
B.醋酸为弱电解质,应写成化学式;
C.硫化亚铁不溶于水,应写成化学式;
D.碳酸钙不溶于水,与酸反应生成二氧化碳气体.
解答:A.铁跟稀硫酸反应的离子方程式为Fe+2H+=Fe2++H2↑,故A正确;
B.醋酸为弱电解质,跟氢氧化钾溶液反应的离子方程式为CH3COOH+OH-=CH3COO-+H2O,故B正确;
C.硫化亚铁不溶于水,加入盐酸反应的离子方程式为FeS+2H+=H2S↑+Fe2+,故C错误;
D.碳酸钙不溶于水,溶于盐酸中发生反应的离子方程式为CaCO3+2H+=Ca2++H2O+CO2↑,故D正确.
故选C.
点评:本题考查离子方程式的书写,为高考常见题型,综合考查学生元素化合物知识的综合应用能力,注意把握离子方程式的书写方法,以及反应物和生成物的化学式和离子符号的判断,离子反应要符合反应的实际,题目难度不大.
本题难度:困难
5、选择题 下列物质中既含离子键又含非极性共价键的是( )
A.NH4Cl
B.KOH
C.Na2O2
D.H2S
参考答案:A、NH4C1中铵根离子与氯离子以离子键结合,N、H之间以极性共价键结合,故A不选;
B、KOH中钾离子与氢氧根离子以离子键结合,O、H之间以极性共价键结合,故B不选;
C、Na2O2中钠离子与过氧根离子以离子键结合,O、O之间以非极性键结合,故C选;
D、H2S中只有H-S极性共价键,故D不选;
故选C.
本题解析:
本题难度:简单