时间:2017-11-11 04:07:54
1、实验题 实验是进行化学研究的重要手段之一。请回答下列问题:
(1)下列实验操作,错误的是________________ ____(填写序号)。
____(填写序号)。
a. 用纸槽往试管里装粉末状药品时,试管应先横放再直立
b. 称取氢氧化钠固体时,应将氢氧化钠固体直接放在左边托盘内,右边托盘放砝码
c. 试管、烧杯、量筒、集气瓶都不能用酒精灯直接加热
d. 用试纸检验气体性质时,手拿着试纸经水润洗后靠近气体观察试纸颜色的变化
用试纸检验气体性质时,手拿着试纸经水润洗后靠近气体观察试纸颜色的变化
e.闻气体气味时,应取一瓶盛满气体的集气瓶,稍打开玻璃片,用手轻轻扇地在瓶口扇动,使极少量的气体飘进鼻孔,闻气味
(2)实验室需要450mL 0.1mol·L-1NaOH溶液和500mL 0.5 mol·L-1硫酸溶液。请回答下列问题:
①在下图所示仪器中,配制上述溶液肯定不需要的是_________(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器有?。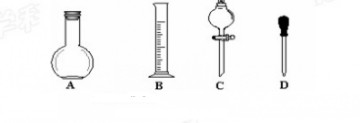
②在容量瓶的使用方法中,下列 91Exam.org操作正确的是____________(填写序号)。
a.使用容量瓶前检验是否漏水
b.容量瓶用水洗净后,再用待配溶液洗涤
c.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流注入容量瓶中,然后加蒸馏水。
d.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
③配制450 mL 0.1mol·L-1 NaOH溶液的实验步骤如下:
a.计算 应称取氢氧化钠固体的质量为________g。
应称取氢氧化钠固体的质量为________g。
b.称量氢氧化钠固体。
c.将烧杯中的溶液注入容量瓶,并用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也注入容
量瓶。
d.用适量的蒸馏水溶解称量好的氢氧化钠固体,冷却。
e.盖好瓶塞 ,反复上下颠倒,摇匀。
,反复上下颠倒,摇匀。
f.继续向容量瓶中加蒸馏水至刻度线下1~2cm时,改用胶头滴管滴加蒸馏水至凹液面与
刻度线相切。
上述步骤的正确操作顺序为_______________________(用序号表示)。
④根据计算得知,需用 量筒量取质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为
量筒量取质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为
?mL,如果 实验室有15mL、20mL、50mL量筒,应选用?mL量筒最好。
实验室有15mL、20mL、50mL量筒,应选用?mL量筒最好。
参考答案:(16分)
(1) bcd(2分)
(2)① A C(2分)?烧杯、玻璃棒、500mL容量瓶(2分,每少一种扣1分)②?ad(2分)?③2.0(2分)?abdcfe(2分)④13.6(2分)?15( 2分)
2分)
本题解析:略
本题难度:简单
2、实验题 (10分)
现用质量分数为36.5%、密度为1.20 g·cm-3的浓盐酸来配制100 mL 1.5 mol/L的稀盐酸。可供选择的仪器有:①玻璃棒②烧瓶③烧杯④胶头滴管⑤量筒⑥容量瓶⑦托盘天平⑧药匙。请回答下列问题:
(1)上述仪器中,在配制稀盐酸时用不到的有?(填代号)。
(2)经计算,需浓盐酸的体积为?。
现有①10 mL?②20 mL?③50 mL?④100 mL四种规格的量筒,取用浓盐酸应选用的量筒是?(填代号)。
(3)在配制过程中,其他操作都准确,下列操作中:错误的是?,能引起误差偏高的有?(填序号)。
①洗涤量取浓盐酸后的量筒,并将洗涤液转移到容量瓶中
②稀释后的盐酸在空气中放置过久
③定容时,加蒸馏水超过标线,又用胶头滴管吸出
④转移前,容量瓶中含有少量蒸馏水
⑤定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
⑥定容时,俯视标线
参考答案:(1)②⑦⑧? (2)12.5mL?②? (3)①②③⑤⑥?①⑥
本题解析:略
本题难度:一般
3、选择题 下列有关实验操作及实验结论正确的是
A.金属钠着火,可用泡沫灭火器扑灭
B.用10 mL量筒准确量取7.50 mL稀硫酸
C.用四氯化碳萃取溴水中的溴时,将溴的四氯化碳溶液从分液漏斗下口放出
D.向淀粉溶液中加入稀硫酸,加热几分钟后冷却,再加入新制的Cu(OH)2悬浊液,加热,没有砖红色沉淀生成,证明淀粉没有水解成葡萄糖
参考答案:C
本题解析:A、金属钠与氧气反应所生成的过氧化钠可以与二氧化碳气体反应生成氧气,从而帮助燃烧,错误;B、用10 mL量筒只能粗略量取7.5 mL稀硫酸,因为量筒本身就是一个粗略的量具,只能精确到小数点后一位数字,错误;C、正确;D、没有砖红色沉淀,可能是因为没有中和酸的缘故。错误。
本题难度:一般
4、填空题 某同学在用托盘天平称量氯化钠时,物质和砝码放颠倒了,他要称量10.3克氯化钠,实际称量的氯化钠的质量为?g
参考答案:9.7g
本题解析:托盘天平称量时应该是左物右码,当物质和砝码放颠倒后,称量所得的数值小数点后为游码的读数,故本题实际称量的氯化钠的质量为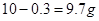 。
。
点评:主要考查托盘天平的正确使用,应遵循“左物右码”的原则,解题的关键是要找出游码的读数,从而快速作答。
本题难度:简单
5、选择题 下述实验操作与预期实验目的或所得实验结论不一致的是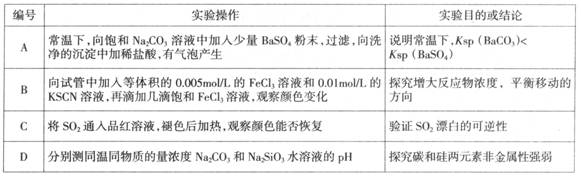
参考答案:A
本题解析:溶液中能否产生沉淀,关键是溶液中有关离子浓度的幂之积是否大于溶度积常数,只要大于相应的溶度积常数,则一定会产生沉淀,而与相应的溶度积常数大小并没有直接的关系,实际上碳酸钡的溶度积常数大于硫酸钡的溶度积常数,A不正确,其余都是正确的,答案选A。
本题难度:简单