时间:2017-11-11 03:49:02
1、选择题 Li- Al/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为:2Li++ FeS +2e-=Li2S+Fe 有关该电池的下列说法中,正确的是
[? ]
A.Li-Al在电池中作为负极材料,该材料中Li的化合价为+1价
B.该电池的电池反应式为:2Li+FeS=Li2S+Fe
C.负极的电极反应式为:Al-3e-=Al3+
D.充电时,阴极发生的电极反应式为:Li2S+ Fe-2e-=2Li++FeS
2、选择题 如图是工业电解饱和食盐水的装置示意图,下列有关说法中不正确的是(? )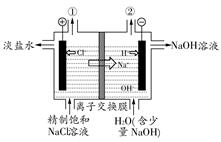
A.装置中出口①处的物质是氯气,出口②处的物质是氢气
B.该离子交换膜只能让阳离子通过,不能让阴离子通过
C.装置中发生反应的离子方程式为:2Cl-+2H+ Cl2↑+H2↑
Cl2↑+H2↑
D.该装置是将电能转化为化学能
3、选择题 用石墨作电极电解CuCl2溶液,当通电一段时间后,收集到2.24 L气体(标准状况)。下列有关说法正确的是?(?)
A 阳极生成的铜?
B 上述电解过程中共转移0.2 mol电子
C 电解得到的Cu的物质的量为0.5 mol?
D 电解后溶液呈碱性
4、选择题 石墨作电极电解下列溶液,阴阳两极产生的气体体积比为2:1,且电解液pH增大的是
[? ]
A.KCl
B.NaOH
C.Na2SO4
D.H2SO4
5、选择题 铝阳极氧化处理后形成的氧化膜比铝的天然氧化膜耐磨性、耐腐蚀性及装饰性有明显的提高,工业中以铝为阳极,置于硫酸溶液中电解,装置如图所示,下列说法正确的是
A.阳极电极方程式为: Al―3e―+6OH―=Al2O3+H2O
B.随着电解的进行,溶液的pH逐渐增大
C.当阴极生成气体3.36L(标况)时,阳极增重2.4g
D.电解过程中H+移向Al电极