时间:2017-11-11 03:40:56
1、选择题
A.推广使用无磷洗涤剂
B.集中掩埋废旧电池
C.城市生活垃圾分类处理
D.在农村倡导建造沼气池
参考答案:B
本题解析:本题考查环保知识,较易题。电池的危害主要是其电解质溶液中的重金属离子对土壤和水体产生污染,集中掩埋废旧电池依然会产生污染。故选B。
本题难度:一般
2、选择题 下列有关环境相关说法中正确的是(?)
A.PH小于7的雨水称为酸雨
B.白色污染即白色废弃物造成的污染
C.SO2、NO2也能破坏臭氧层
D.CO2是引起温室效应的主要原因
参考答案:C
本题解析:PH小于5.6的雨水称为酸雨;白色污染是指废弃塑料造成的污染;由于SO2、NO2均具有还原性,且能与O3反应,故都能破坏臭氧层。
【误区警示】同学们都知道氟里昂是破坏臭氧层的罪魁祸首,但往往忽视还原性物质与O3反应而对臭氧层的破坏。
本题 难度:一般
3、选择题 下列有关酸雨的说法中错误的是
A.酸雨是指pH小于7的雨水
B.酸雨是由于大气中的二氧化硫和二氧化氮溶于雨水而形成的
C.酸雨严重危害生物体生命安全;还会加速交通设施及电信电缆的腐蚀
D.防治酸雨的根本措 施是杜绝污染源
施是杜绝污染源
参考答案:A
本题解析:略
本题难度:简单
4、填空题 【化学――选修2化学与技术】
生产自来水的流程图所示。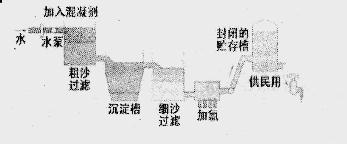
(1) FeSO4・7H2O是常用的混凝剂,它在水中最终生成??沉淀。
(2)实验室过滤操作所用到的玻璃仪器是??。
(3)我们有时感觉自来水“有漂白粉的气味”,是因为使用了氯气消毒,请写出有关化学方程下列物质中,?(填写序号)可以作为氯气的代用品。
①臭氧?②NH3(溶液)?③K2FeO4?④SO2
(4)有些地区的天然水中含有较多的钙、镁离子。用离子交换树脂软化硬水时,先后把水通过分别装有?离子交换树脂和?离子交换树脂的离子交换柱(填“阴”或 “阳”)。
(5)测定水中的溶解氧:量取20mL水样,迅速加入MnSO4和KOH的混合溶液,再加入KI溶液,立即塞好塞子,振荡使其完全反应。打开塞子,迅速加入适量硫酸溶液,此时有碘单质生成。用0.010mol/L Na2S2O3溶液滴定生成的碘,消耗了6.00mL Na2S2O3溶液。已知在碱性溶液中,氧气能迅速氧化Mn2+,生成物在酸性条件下可以将碘离子氧化为碘单质,本身重新还原为Mn2+。
上述过程发生的反应可表示为:
2Mn2++4OH-+O2=2MnO(OH)2
MnO(OH)2+2I-+4H+=I2+Mn2++3H2O
I2+2S2O32-=2I-+S4O62-
水中的溶解氧量为?(以mg・L-l为单位)。
参考答案:(除第(5)小题3分,其余每空2分,共15分)。
(1)Fe(OH)3
(2)漏斗、烧杯、玻璃棒
(3)Cl2+H2O HCl+HClO?①③
HCl+HClO?①③
(4)阳、阴
(5)24.0
本题解析:(1)FeSO4・7H2O是常用的混凝剂,它在水中水解生成氢氧化亚铁,氢氧化亚铁与空气中的氧气反应最终生成Fe(OH)3
(2)实验室过滤操作所用到的玻璃仪器是漏斗、烧杯、玻璃棒;
(3)使用氯气消毒,是因为氯气与水反应生成的次氯酸具有强氧化性,反应原理为Cl2+H2O HCl+HClO;所以能替代氯气用于消毒的物质是K2FeO4,铁为+6价,所以K2FeO4具有强氧化性;或者臭氧,臭氧也具有强氧化性,其他2种物质一般不作氧化剂,所以最佳选择是①③;
HCl+HClO;所以能替代氯气用于消毒的物质是K2FeO4,铁为+6价,所以K2FeO4具有强氧化性;或者臭氧,臭氧也具有强氧化性,其他2种物质一般不作氧化剂,所以最佳选择是①③;
(4)通过阴离子交换树脂后生成OH-,OH-会与钙、镁离子反应生成沉淀,影响阳离子交换树脂发挥作用,故先通过阳离子交换树脂再通过阴离子交换树脂;
(5)由所给化学方程式可得氧气与Na2S2O3的物质的量的比例关系为:O2~4S2O32-,已知n(S2O32-)=0.01mol/L×0.006L=6×10-5mol,则n(O2)=1/4×6×10-5mol=1.5×10-5mol,m(O2)=1.5×10-5mol×32g/mol=48×10-5g=0.48mg,则水中的溶解氧量为0.48mg/0.02L=24mg・L-l
本题难度:一般
5、选择题 目前,常用的垃圾处理的方法有
A.堆肥法
B.卫生填埋
C.焚烧
D.垃圾分类回收
参考答案:ABCD
本题解析:常用的垃圾处理方法分别有堆肥法,卫生填埋,焚烧,垃圾分类回收等,同时,最经常使用的是焚烧和垃圾分类回收。
点评:本题考查的是常用的垃圾处理方法,题目难度不大,把握相关知识点与概念即可
本题难度:一般