ʱ��:2017-11-11 03:17:59
1������� ԭ�����������IJ��ֶ���������Ԫ�ص�ԭ�Ӱ뾶�������±���
| Ԫ�� | A | B | D | E | F | G | M | N | P |
| ԭ�Ӱ뾶/nm | 0.077 | 0.070 | 0.066 | 0.064 | 0.186 | 0.160 | 0.143 | 0.104 | 0.099 |
�ο��𰸣���1����ԭ�Ӱ뾶��ϵ��֪A��B��D��EΪ�ڶ�����Ԫ�أ���Ϊ�ǽ�����Ӧ�ֱ�ΪC��N��O��FԪ�أ�F��G��M��N��PΪ��������Ԫ�أ�����A��B��D��E����F��G��M�е��κ�һ��Ԫ��ͬ�壬��F��G��MӦ�ֱ�ΪNa��Mg��AlԪ�أ�����A��B��D��E��N��P�����λ�ÿ�֪��NΪSԪ�أ�PΪClԪ�أ����ԣ��������Ӧ��Ԫ��Ϊ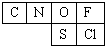
��
�ʴ�Ϊ��
��
?��2��BΪNԪ�أ�ԭ������Ϊ7��ԭ�Ӻ�����2�����Ӳ㣬����������Ϊ5����λ�ڵڶ�����VA�壬AD2ΪCO2��Ϊ���ۻ��������ʽΪ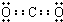
��
�ʴ�Ϊ���ڶ�����VA�壻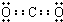
��
��3��M������������ˮ������Al��OH��3��θ�����Ҫ�ɷ�Ϊ���ᣬ���߷�����Ӧ��Al��OH��3+3H+�TAl3++3H2O��
�ʴ�Ϊ��Al��OH��3+3H+�TAl3++3H2O��
��4��SO2��CO2�������ƣ�Mg����ȼ�գ�2Mg+CO2?��ȼ?.?2MgO+C�����У�2Mg+SO2?��ȼ?.?2MgO+S����Mg��S��Ӧ����MgS��������ӦΪ��Mg+S?��ȼ?.?MgS������ܵIJ�����MgO��MgS��S��
�ʴ�Ϊ��MgO��MgS��S��2Mg+SO2?��ȼ?.?2MgO+S��Mg+S?��ȼ?.?MgS��
���������
�����Ѷȣ�һ��
2��ѡ���� ��������һ����ȷ����
[? ]
A�������ӻ������в����ܴ��ڷǼ��Թ��ۼ�
B���ڹ��ۻ������в����ܴ������Ӽ�
C����ͬ�ַǽ���Ԫ����ɵĶ�ԭ�ڷ��ӣ����еĻ�ѧ��һ��ȫ���Ǽ��Լ�
D���Ǽ��Լ�ֻ������˫ԭ�ӵ��ʵķ�����
�ο��𰸣�B
���������
�����Ѷȣ���
3������� (1)��������10�����ʵ������գ���O2����H2����NH4NO3����K2O2����Ba(OH)2����CH4�� ��CO2��
��NaF����NH3����I2�������ɷǼ��Լ��γɵķǼ��Է�����___________���ɼ��Լ��γɵķǼ��Է���
��_________���������Ӽ����зǼ��Լ�����________���������Ӽ����м��Լ�����________��
(2)X��Y��������Ԫ�����γ�XY2�ͻ������֪XY2�й���38�����ӣ���XY2Ϊ����Ԫ���γɵ����ӻ�����仯ѧʽΪ____________����XY2Ϊ���ۻ��������ṹʽΪ____________��
(3)�Ȼ������������ʷdz����⣬���Ȼ������۵�Ϊ190��(2.02��103Pa)������180��Ϳ�ʼ�������ݴ��� �ϣ��Ȼ�����____������ۡ������ӡ������������֤������ж���ȷ��ʵ��������____________________��
�ο��𰸣�(1)�٢ڢ⣻�ޢߣ��ܣ��ۢ�
(2)CaF2��S=C=S
(3)���ۣ��Ȼ���������״̬�²��ܵ���
���������
�����Ѷȣ�һ��
4��ѡ���� X��Y��Z��W��R���Ƕ�����Ԫ�أ�������Ԫ�����ڱ��е����λ����ͼ��ʾ������W����������ϼ���������ϼ۾���ֵ��ȣ�����˵����ȷ���ǣ�������
| X Y Z W R |
�ο��𰸣�W����������ϼ���������ϼ۾���ֵ��ȣ���������ϼ���������ϼ۾���ֵ֮��һ������8������W��λ�ã���֪W�裬ZΪAl��YΪNa��RΪS��XΪO��
A��X��Y�γɵĻ������������ƺ������ƣ����й������ƿ��ԺͶ�����̼��ˮ��Ӧ��������������Ϊ��������Դ����A��ȷ��
B��Z��W��R�ֱ���X�γɵĻ������ˮ����Ϊ��Al��OH��3��H2SiO3��H2SO4�����Ƿֱ����ڼ���ᡢǿ�ᣬ��B����
C��O��S��Si�ĵõ�������˳��Ϊ��O��S��Si������̬�⻯������ȶ��ԣ�H2O��H2S��SiH4����C��ȷ��
D���ڻ����������ƺ������У������Ӱ뾶С�������Ӱ뾶����D����
��ѡAC��
���������
�����Ѷȣ�һ��
5��ѡ���� ���л�ѧ���������ȷ���ǣ�������
A����ԭ�ӵĽṹʾ��ͼ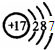
B��CH4�ĵ���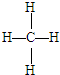
C����ϩ�Ľṹ��ʽCH2CH2
D���Ҵ��Ľṹ��ʽC2H6O
�ο��𰸣�A��Cl��������Ϊ17����ԭ�ӵĽṹʾ��ͼ ����A��ȷ��
����A��ȷ��
B������Ľṹʽ�С�-����ʾһ�Թ��õ��Ӷԣ�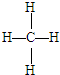 Ϊ�ṹʽ����B����
Ϊ�ṹʽ����B����
C���ṹ��ʽ�й����Ų���ʡ�ԣ�����ϩ�Ľṹ��ʽΪCH2=CH2����C����
D���ṹ��ʽ�����ֹ����ţ����Ҵ��Ľṹ��ʽΪCH3CH2OH����D����
��ѡA��
���������
�����Ѷȣ�һ��