ʱ��:2017-11-11 02:50:18
1������� (1)KAl(SO4)2��Һ���ɺ�õ��Ĺ���������____��ԭ����______ ��
(2)̼���Ⱶ��Һ���ɺ�õ��Ĺ�����____��ԭ����___��
(3)����������Һ���ɺ�õ��Ĺ���������_____��ԭ����___��
(4)�ڸ�����Ȼ��������м���ˮ���Ȼ�þ(MgCl2��6H2O)���壬�õ��Ĺ���������___��ԭ����_____��
�ο��𰸣�(1) KAl(SO4)2 ������Al3+ˮ�⣬����H2SO4Ϊ�̷е��ᣬ�����Ȼ�ǵõ�KAl(SO4)2
(2)BaCO3 ̼���Ⱶ��ˮ��Һ�����ȷֽ⣬ Ba(HCO3)2 BaCO3+CO2��+H2O
BaCO3+CO2��+H2O
(3)Na2SO4 �������������ɵĹ����в��ϱ��������������Na2SO4��2Na2SO3+ O2==2Na2SO4
(4)��ˮMgCl2 ���Ȼ��������У�HCl���� Mg2+��ˮ���Ҵ���ˮ���������յõ���ˮMgCl2
���������
�����Ѷȣ�һ��
2��ѡ���� ��0.5mol��������������500mlˮ�У�������������Ŀ������
A��CaCO3
B��CH3COONa
C��NH3
D��Na2SO3
�ο��𰸣�D
�����������
�����Ѷȣ���
3������� ������SOCl2��һ��Һ̬������е�Ϊ77�棬��ʢ��10mL����ƿ��С�ĵμ�8��10��SOCl2���ɹ۲� ������ˮ�ⷴӦ��Һ���а����ʹ��д̼�����ζ�������ݳ����������ʹ����Ʒ����Һ����ֽ��ɫ����������ƿ���Ȱ�����ʧ������Һ�еμ�AgNO3��Һ���в�����HNO3�İ�ɫ����״����������
(1)��������ʵ�飬д��SOCl2��ˮ��Ӧ�Ļ�ѧ����ʽ____________��
(2) AlCl3��Һ�������յò�����ˮAlCl3������SOCl2��AlCl3��H2O��Ϲ��ȣ��ɵõ���ˮAlCl3����ԭ����______________��
�ο��𰸣�(1)SOCl2+H2O==SO2+2HCl
(2)��AlCl3��Һ�������գ� AlCl3��ˮ�д�������ƽ�⣺AlCl3+3H2O Al(OH)3+3HCl, ���ɺ����չ����У�HCl�ӷ���Al(OH)3�ֽ⣺2Al(OH)3
Al(OH)3+3HCl, ���ɺ����չ����У�HCl�ӷ���Al(OH)3�ֽ⣺2Al(OH)3 Al2O3+3H2O������˹��������ҪΪAl2O3��SOCl2��ˮ��Ӧ����SO2��HCl��һ����ʹˮ�����ʵ������٣���һ�������ɵ�������AlCl3��ˮ�⣬����SOCl2��AlCl3��6H2O���ȿɵ�AlCl3
Al2O3+3H2O������˹��������ҪΪAl2O3��SOCl2��ˮ��Ӧ����SO2��HCl��һ����ʹˮ�����ʵ������٣���һ�������ɵ�������AlCl3��ˮ�⣬����SOCl2��AlCl3��6H2O���ȿɵ�AlCl3
���������
�����Ѷȣ�һ��
4��ѡ����
A���Ȼ���
B��̼������
C������þ
D���������
�ο��𰸣�C
������������⿼���˼������ʵ���Һ��������ȶ��ԡ�AlCl3����ˮ�⣬����Һ�������ɺ��ܵõ�Al(OH)3�ֽ����Al2O3��NaHCO3�����KMnO4������ȶ��ֽ⣬ֻ��MgSO4���ȶ���
�����Ѷȣ���
5��ѡ���� ��֪����ͬ����������ǿ��˳��Ϊ��CH3COOH>H2CO3>HCN>HCO3�������б�������ȷ����
A��25��ʱ�������ʵ���Ũ�ȵĸ���ҺpH��ϵΪ��pH(Na2CO3)��pH(NaCN)��pH(NaHCO3)��pH(CH3COONa)
B��a mol��L��1 HCN��Һ��bmol��L��1 NaOH��Һ�������Ϻ�������Һ�У�c(Na+)��c(CN��)����aһ������b
C��0.1mol��L��1��Na2CO3��Һ�У�c(OH��)��c(H+)��c(HCO3��)��c(H2CO3)
D��25��ʱ��pH��4.75��Ũ�Ⱦ�Ϊ0.1mol��L��1��CH3COOH��CH3COONa�����Һ��c(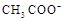 )+c(
)+c(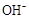 )<c(CH3COOH)+c(H+)
)<c(CH3COOH)+c(H+)
�ο��𰸣�C D
���������A����ȷ��CH3COOH>H2CO3>HCN>HCO3������Խǿ��Ӧ����ˮ������Խ���������ʵ���Ũ�ȵĸ���ҺpHԽС��B����ȷ��CN�D����Ҫˮ�⣬��c(Na+)��c(CN��)��HCNһ��Ҫ������aһ������b��C������ȷ�������غ��ʽ��Ϊ��c(OH��)��c(H+)��c(HCO3��)��2c(H2CO3)��D������ȷ��
�����Ѷȣ�һ��