时间:2017-11-11 02:28:57
1、选择题 下列叙述正确的是( )
A.醋酸溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a>b
B.25℃l.0×10-1mol/L盐酸的pH=3.0,1.0×10-8mol/L盐酸的pH=8.0
C.lmLpH=1的盐酸与10mLNaOH溶液混合后pH=7,则NaOH溶液的pH=11
D.pH=1的盐酸溶液稀释100倍后,pH=3
2、选择题 在100mL0.1mol/L 的醋酸溶液中,欲使醋酸的电离程度增大,H+浓度减小,可采用方法是( ) ?
A?加热。?B?加入0.1mol/L 的醋酸溶液100mL。
C?加入少量的0.5mol/L的硫酸。? D?加入少量1mol/L 的NaOH溶液。
3、填空题 2013年1月27日百度新闻资讯中报道,活性氧化锌是一种多功能性的新型无机材料,其颗粒大小约在1~100纳米。云南化工冶金研究所采用湿化学法(NPP-法)制备纳米级活性氧化锌,可用各种含锌物料为原料,采用酸浸出锌,经过多次净化除去原料中的杂质,然后沉淀获得碱式碳酸锌,最后焙解获得活性氧化锌,化学工艺流程如下: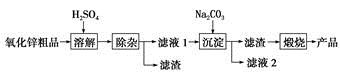
(1)通过________可以检验流程中滤液2中含有Na+。
(2)上述流程图中pH=12的Na2CO3溶液中c(CO32- )=0.50 mol/L,c(HCO3- )=1×10-2 mol/L,则c(Na+)∶c(OH-)=________。
(3)“溶解”后得到的酸性溶液中含有Zn2+、SO42- ,另含有Fe2+、Cu2+等杂质。先加入________(填“Na2CO3”或“H2SO4”)调节溶液的pH至5.4,然后加入适量KMnO4,Fe2+转化为Fe(OH)3,同时KMnO4转化为MnO2。经检测溶液中Fe2+的浓度为0.009 mol·L-1,则每升溶液中至少应加入________mol KMnO4。
(4)已知常温下,Cu(OH)2的溶度积常数Ksp=2×10-20。溶液中杂质Cu2+浓度为0.002 mol·L-1,若要生成沉淀,则应调节溶液的pH大于________。
(5)“沉淀”得到ZnCO3·2Zn(OH)2·H2O,“煅烧”在450~500 ℃下进行,“煅烧”反应的化学方程式为:_____________________________________。
4、选择题 已知下面三个数据:7.2×10-4、4.6×10-4、 4.9×10-10分别是下列有关的三种酸的电离常数,若已知下列反应可以发生: NaCN+ HNO2==HCN+NaNO2? NaCN + HF==HCN+NaF? ?NaNO2 + HF=HNO2 +NaF 由此可判断下列叙述不正确的是
A.K(HF) =7.2×10-4
B.K(HNO2) =4.9×10-1
C.根据其中两个反应即可得出三种酸的强弱顺序为:HF> HNO2>HCN
D.K(HCN)
5、填空题 (12分)Ⅰ、现有常温条件下甲、乙、丙三种溶液,甲为0.1 mol·L-1的NaOH溶液,乙为0.1 mol·L-1的HCl溶液,丙为0.1 mol·L-1的CH3COOH溶液,试回答下列问题:
(1)甲溶液的pH=________;
(2)丙溶液中存在电离平衡为______________________(用电离平衡方程式表示);
(3)甲、乙、丙三种溶液中由水电离出的c(OH-)的大小关系为_________;
Ⅱ、某一元弱酸(用HA表示)在水中的电离方程式是HA