时间:2017-11-11 02:24:43
1、选择题 有甲、乙两种醋酸稀溶液,测得甲的pH=2,乙的pH=3.下列推断中正确的是( )
A.物质的量浓度c(甲)=10c(乙)
B.甲中由水电离产生的H+的物质的量浓度是乙的0.1倍?
C.中和等物质的量浓度等体积的NaOH溶液需甲、乙两酸的体积V(乙)=10V(甲)
D.甲中c(OH-)为乙中c(OH-)的10倍
参考答案:B
本题解析:
本题难度:一般
2、填空题 为了证明醋酸是弱电解质,甲、乙、丙、三人分别选用下列试剂进行实验:
0.1 mol·L-1醋酸溶液、pH=3的盐酸、pH=3的醋酸、、蒸馏水、锌粒、pH试纸等。
(1)甲取出10 mL0.1 mol·L-1醋酸溶液,用pH试纸测出其pH=a,确定醋酸是弱电解质,则a应该满足的关系是_________,理由是__________________________________。
(2)乙将pH=3醋酸和盐酸,各取1 mL,用蒸馏水稀释到100 mL,然后用pH试纸
分别测定两溶液的pH,则可认定醋酸是弱电解质,判断的依据是______________________________。
(3)丙分别取pH=3的盐酸和醋酸10 mL,然后分别加入质量相同的锌粒,醋酸放出H2的平均速率?(填“快”或“慢”),则认定醋酸是弱电解质,。
参考答案:(1) a>1?因为醋酸为弱酸部分电离?(2)盐酸的pH=5,醋酸的pH<5或醋酸在稀释过程中电离出H+,使PH变化小于盐酸。? (3)快
本题解析:醋酸是弱电解质,可测定一定浓度的pH、测定盐溶液的pH、醋酸的电离平衡移动、稀释时pH的变化等来分析;(1)测0.1 mol·L-1醋酸溶液的pH,若pH大于1,醋酸不能完全电离,则可证明醋酸为弱电解质;(2)pH=3醋酸和盐酸,各取1 mL,用蒸馏水稀释到100 mL,稀释100倍,测其pH,盐酸的pH变为5,若醋酸的pH<5,说明稀释促进醋酸电离,使H+浓度增大,证明醋酸溶液中存在电离平衡,为弱电解质;(3)当pH相同、体积相同时,盐酸完全电离,醋酸存在电离平衡,则分别加入足量锌,醋酸存在电离平衡向右移动,使得反应过程中醋酸中H+浓度大于盐酸,反应速率快。
本题难度:一般
3、选择题 已知同温同浓度时,①H2CO3比H2S的电离(“-”级电离)常数大,②H2S比HCO3-的电离常数大(即H2S的K1比H2CO3的K2大),根据酸与盐的反应规律,下列反应中不正确的是
[? ]
A.Na2CO3+H2S=NaHCO3+NaHS
B.Na2S+H2O+CO2=NaHS+NaHCO3
C.2NaHCO3+H2S=Na2S+2H2O+2CO2
D.NaHS+H2O+CO2=NaHCO3+H2S
参考答案:C
本题解析:
本题难度:一般
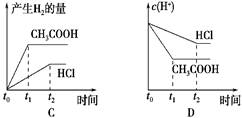
4、选择题 向1 L pH=2的盐酸和醋酸溶液中,分别投入0.65 g锌粒,则下图中比较符合客观事实的是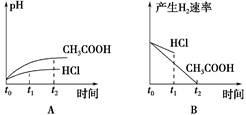 ?
?
参考答案:C
本题解析:0.65 g锌粒是0.01mol,盐酸是强酸,起物质的量是0.01mol,所以盐酸不足,生成氢气是0.005mol。醋酸是弱酸,其浓度大于0.01mol/L,所以锌不足,即醋酸产生的氢气多。由于在反应过程中,产生会继续电离出氢离子,所以醋酸的反应速率快,答案选C。
本题难度:一般
5、选择题 氢氰酸(HCN)的下列性质中,可以证明它是弱电解质的是
A.1mol/L氢氰酸溶液的pH约为3
B.HCN易溶于水
C.10 mL1mol/LHCN恰好与10 mL 1mol/L NaOH溶液完全反应
D.HCN溶液的导电性比强酸溶液的弱
参考答案:A
本题解析:A可以,常温下,如果HCN是强电解质,1mol/LHCN溶液,PH应该等于0
B错误,溶解性与电解质强弱没有直接关系。
C错误,恰好完全反应并没有说明溶液的酸碱性情况。
D错误,导电能力强弱与电解质强弱无直接关系。
本题难度:一般