ʱ��:2017-11-11 02:15:48
1������� ��������±ʯ(K2SO4��MgSO4��2CaSO4��2H2O)���ڡ�������ˮ�д��������ܽ�ƽ�⣺
K2SO4��MgSO4��2CaSO4��2H2O(s) 2Ca2����2K����Mg2����4SO42-��2H2O��Ϊ�ܳ�����ü���Դ���ñ���Ca(OH)2��Һ�ܽ���±ʯ�Ʊ�����أ������������£�
2Ca2����2K����Mg2����4SO42-��2H2O��Ϊ�ܳ�����ü���Դ���ñ���Ca(OH)2��Һ�ܽ���±ʯ�Ʊ�����أ������������£�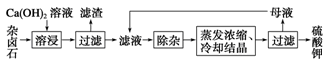
��1��������Ҫ�ɷ���________��CaSO4�Լ�δ����±ʯ��
��2���û�ѧƽ���ƶ�ԭ������Ca(OH)2��Һ���ܽ���±ʯ����K����ԭ��
?��
��3�������ӡ������У��ȼ���?��Һ��������Ȳ������ˣ��ټ���?��Һ����ҺpH�����ԡ�
��4����ͬ�¶��£�K���Ľ���Ũ�����ܽ�ʱ��Ĺ�ϵ����ͼ����ͼ�ɵã������¶����ߣ�
��?��
��?��
���ܽ�����K����ƽ��Ũ������
��5�������Կ�����̼����Ϊ�ܽ��������ܽ������лᷢ����CaSO4(s)��CO32- CaCO3(s)��SO42-����֪298 Kʱ��Ksp(CaCO3)��2.80��10��9��Ksp(CaSO4)��4.90��10��5��������¶��¸÷�Ӧ��ƽ�ⳣ����K��?��
CaCO3(s)��SO42-����֪298 Kʱ��Ksp(CaCO3)��2.80��10��9��Ksp(CaSO4)��4.90��10��5��������¶��¸÷�Ӧ��ƽ�ⳣ����K��?��
�ο��𰸣���1��Mg(OH)2(1��)?��2������Ca(OH)2��Һ��Mg2����OH���������Mg(OH)2������Mg2��Ũ�ȼ�С��ƽ�������ƶ���K������(2��)?��3��K2CO3(1��) ?H2SO4(1��)
��4�����ܽ�ƽ�������ƶ�(1��)?��K�����ܽ���������(1��)?��5�� K��1.75��104��(2��)
�����������1����������ˮ�д��ڳ����ܽ�ƽ��K2SO4��MgSO4��2CaSO4��2H2O(s) 2Ca2����2K����Mg2����4SO42-��2H2O��Ϊ�ܳ�����ü���Դ���ñ���Ca(OH)2��Һ�ܽ���±ʯ�Ʊ�����أ����������Ӻ�þ���ӽ������������þ������ͬʱ���������࣬��������Ƴ�����������������Ҫ�ɷ�ΪMg(OH)2��CaSO4�Լ�δ����±ʯ��
2Ca2����2K����Mg2����4SO42-��2H2O��Ϊ�ܳ�����ü���Դ���ñ���Ca(OH)2��Һ�ܽ���±ʯ�Ʊ�����أ����������Ӻ�þ���ӽ������������þ������ͬʱ���������࣬��������Ƴ�����������������Ҫ�ɷ�ΪMg(OH)2��CaSO4�Լ�δ����±ʯ��
��2��Ca(OH)2��Һ���ܽ���±ʯ����K+��ԭ�������������DZ�����Һ����������������Ӻ�þ���ӽ������������þ�������ٽ�ƽ�����ƣ�����K+��
��3���������ӡ�������Ҫ�dz�ȥ�����ӣ����ݳ���ԭ���������µ����ʣ�������ȡ��Ŀ�����Ʊ�����أ����Լ�����Լ����ڳ�ȥ���������µ����ʣ���˼������K2CO3�������ӣ����˺�������������ԣ���ȥ̼��ؼ��ɡ�
��4��������ͬ�¶��£�K+�Ľ���Ũ�����ܽ�ʱ��Ĺ�ϵ���¶�Խ��K+�Ľ���Ũ��Խ���ܽ�ʱ��Խ�̣���Ӧ����Խ�ﵽƽ��Խ�죬��ͼ���з����õ��Ľ���Ϊ�����ܽ�ƽ�������ƶ�����K�����ܽ���������
��5���ܽ������лᷢ����ӦCaSO4(s)��CO32- CaCO3(s)��SO42-��CaCO3(s)
CaCO3(s)��SO42-��CaCO3(s) Ca2++CO32-��CaSO4(s)
Ca2++CO32-��CaSO4(s) Ca2++SO42-����������ơ�̼����ܶȻ������ļ������ʽ��ת����ϵ�и�������ͬ���㣬��Ӧ��ƽ�ⳣ��K��
Ca2++SO42-����������ơ�̼����ܶȻ������ļ������ʽ��ת����ϵ�и�������ͬ���㣬��Ӧ��ƽ�ⳣ��K��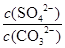 ��
��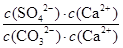 ��
��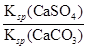 ��
��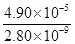 ��1.75��104��
��1.75��104��
�����Ѷȣ�һ��
2������� �Ի�����Ϊԭ��������������������к�Fe2O3��SiO2��Al2O3��MgO�ȡ�ʵ����ģ�ҵ���������Ʊ�����(Fe2O3)���������£�
��1���������ijɷ�������������������� �� д�����ܹ���Fe2O3��ϡ���ᷴӦ�����ӷ�Ӧ����ʽ�� ��
��2�����������У�Ϊ��ȷ������Ĵ��ȣ�����������Ҫ������Һ��pH�ķ�Χ��_________��������������������������ʽ����ʱ��Һ��pH���±���
| ������ | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| ��ʼ���� | 2.7 | 3.8 | 7.5 | 9.4 |
| ��ȫ���� | 3.2 | 5.2 | 9.7 | 12.4 |
�ο��𰸣�32�� ��16�֣�(1) Al2O3 Fe2O3 + 6H+ ==2Fe3+ + 3H2O
(2)3��2��3��8 (3) SiO2 Al2(SO4)3 ��4�� 14m/15w
�����������1���������к�Fe2O3��SiO2��Al2O3��MgO�������������������Al2O3���������Ǽ�����������Ժ����ᷴӦ������������ˮ����Fe2O3+3H2SO4=Fe2��SO4��3+3H2O�����ӷ�Ӧ����ʽΪ��Fe2O3 + 6H+ ==2Fe3+ + 3H2O��2�����ݼ������ӳ�����pH��ʹFe3+������ȫ��PHΪ3��2���������ӿ�ʼ����PHΪ3��8�������ѡPH�����3��2��3��8֮�䣻��Ϊ��3��2��3��8����3����������費�����ᷴӦ��������A����Ҫ�ɷݵĻ�ѧʽΪSiO2��δ����������ΪNa+��Mg2+��Al3+����ҺB���Ի��յ�������Na2SO4��Al2��SO4��3��MgSO4����4�������Ʊ������У���Ԫ�����25%�������յõ����������Ϊm kg����Ԫ�ص�����Ϊ(1000m��112/160)��75%=14m/15����ԭ������������Ԫ����������Ϊ14m/15w��
���㣺�������ʵ����ʣ����ӷ���ʽ����д��Ԫ�ؼ��仯��������ʵ�֪ʶ��
�����Ѷȣ�����
3������� ��11�֣�����ʵ�ˮ��Һ�д��ڵ���ƽ�⡣
��1�������dz��������ᡣ
�ٴ�����ˮ��Һ�еĵ��뷽��ʽΪ_________��
�����з����У�����ʹ����ϡ��Һ��CH3COOH����̶��������__________������ĸ��ţ���
a���μ�����Ũ���� b������Һ
c����ˮϡ�� d���������������ƾ���
��2����0.1 mol��L-1NaOH��Һ�ֱ�ζ������Ϊ20.00 mL��Ũ�Ⱦ�Ϊ0.1mol��L-1������ʹ�����Һ���õ��ζ���������ҺpH�����NaOH��Һ������仯�������ζ����ߡ�
�ٵζ������������_____���I������
�ڵζ���ʼǰ��������Һ����ˮ�������c(H+)������_____��
��V1��V2�Ĺ�ϵ��V1_____V2���>������=����<������
��M���Ӧ����Һ�У������ӵ����ʵ���Ũ���ɴ�С��˳����_________��
��3��Ϊ���о������ܽ�ƽ��ͳ���ת����ijͬѧ�������ϲ��������ʵ�顣
���ϣ�AgSCN�ǰ�ɫ��������ͬ�¶��£��ܽ�ȣ�AgSCN > AgI��
| �������� | ���� |
| ����1����2 mL 0.005 mol��L-1 AgNO3��Һ�м���2 mL 0.005 mol��L-1 KSCN��Һ�����á� | ���ְ�ɫ������ |
| ����2��ȡ1 mL�ϲ���Һ���Թ��У��μ�1��2mol��L-1 Fe(NO3)3��Һ�� | ��Һ���ɫ�� |
| ����3������2����Һ�У���������5��3 mol��L-1 AgNO3��Һ�� | ����a����Һ��ɫ��dz�� |
| ����4������1���µ���Һ�м���5��3 mol��L-1 KI��Һ�� | ���ֻ�ɫ������ |
�ο��𰸣���13�֣�δ������Ŀգ�ÿ��1�֣� ��1���� CH3COOH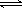 CH3COO��+H+ ��2�֣�
CH3COO��+H+ ��2�֣�
�� b��c��2�֣�©ѡ��1�֣���ѡ���÷֣� ��2���� I �� 0.1mol��L-1������Һ
�� <�� c(CH3COO��)> c (Na+)> c (H+)> c (OH��) ��3���� Fe3++3SCN�� Fe(SCN)3��2�֣�
Fe(SCN)3��2�֣�
�� ���ְ�ɫ���� �� AgSCN(s)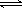 Ag+(aq)+SCN-(aq)��1�֣�������KI����Ϊ�ܽ�ȣ�AgI<AgSCN��Ag+��I-��Ӧ����AgI��ɫ������Ag++I-��AgI����AgSCN���ܽ�ƽ�������ƶ���1�֣�����2�֣�
Ag+(aq)+SCN-(aq)��1�֣�������KI����Ϊ�ܽ�ȣ�AgI<AgSCN��Ag+��I-��Ӧ����AgI��ɫ������Ag++I-��AgI����AgSCN���ܽ�ƽ�������ƶ���1�֣�����2�֣�
�����������1���ٴ�����һԪ���ᣬ����Һ�д��ڵ���ƽ�⣬�������ˮ��Һ�еĵ��뷽��ʽΪCH3COOH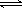 CH3COO��+H+��
CH3COO��+H+��
��a���μ�����Ũ���ᣬ������Ũ���������ƴ�����룬����̶ȼ�С��a����b���������ȣ�����Һ�ٽ����룬����̶�����b��ȷ��c����ˮϡ�ʹֵ��룬����̶�����c��ȷ��d���������������ƾ��壬��������Ũ�ȣ����ƴ�����룬����̶ȼ�С��bc��
��2���ٴ��������ᣬ0.1mol/L������Һ��pH����1����ζ������������I��
�����������������Һ����һԪ��ǿ���ǿ���Ũ����ȵ������¶�ˮ�ĵ���̶�Ӱ������ͬ�ġ�������һԪ���ᣬ��Ũ����������ȵ������£���Һ��������Ũ��С����ˮ�ĵ���̶�Ӱ��С�����ᣬ��ζ���ʼǰ��������Һ����ˮ�������c(H+)������0.1mol/L���ᡣ
���������ƺʹ���ǡ�÷�Ӧʱ���ɵĴ�����ˮ����Һ�Լ��ԣ�Ҫ������Һ�����ԣ������Ӧ�ù���������������������ǡ�÷�Ӧʱ���ɵ��Ȼ��Ʋ�ˮ�⣬��Һ�����ԣ�����V1С��V2��
��M��ʱ�����������Һ���ɵ�Ũ�ȵĴ����ƺʹ��ṹ�ɵģ���Һ�����ԣ����Ӧ����Һ�У������ӵ����ʵ���Ũ���ɴ�С��˳����c(CH3COO��)> c (Na+)> c (H+)> c (OH��)��
��3���� ��������KSCN��Һ��Ӧʹ��Һ�Ժ�ɫ����Ӧ�����ӷ���ʽΪFe3++3SCN�� Fe(SCN)3��
Fe(SCN)3��
����������Һ����KSCN��Һ��Ӧ������ɫ��������������2����Һ�У���������5��3 mol��L-1 AgNO3��Һʱ��Һ����Ȼ����ְ�ɫ������
�۸������Ϸ�����֪��Һ�д���ƽ��AgSCN(s)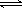 Ag+(aq)+SCN-(aq)������KI����Ϊ�ܽ�ȣ�AgI��AgSCN�����Ag+��I-��Ӧ����AgI��ɫ������Ag++I-��AgI�����Ӷ�����AgSCN���ܽ�ƽ�������ƶ���
Ag+(aq)+SCN-(aq)������KI����Ϊ�ܽ�ȣ�AgI��AgSCN�����Ag+��I-��Ӧ����AgI��ɫ������Ag++I-��AgI�����Ӷ�����AgSCN���ܽ�ƽ�������ƶ���
���㣺����������ʵĵ���ƽ�⡢����ˮ���Լ��ܽ�ƽ���
�����Ѷȣ�һ��
4������� ������ʴ�Ըߣ��ڸ��к����ﵽ12%��Ϊ����֣���ҵ��ұ��������Ҫ������ͼ��ʾ��
�Իش���������
��1�����粽���ķ�Ӧ����ʽΪ��
8Na2CrO4+6Na2S+23H2O��8Cr��OH��3��ʮ3Na2S2O3ʮ22NaOH
�÷�Ӧ����������______���ѧʽ��������?lmolCr��OH��3ʱת�Ƶ��ӵ����ʵ���Ϊ______mol��
��2������IV�е��Cr2O3��������ӦʽΪ______����ʱCr2O3?��״̬Ϊ______��
��3�������£�������������ϡ���ᡢϡ���ᣬ��������Ũ���ᣮ�䲻����Ũ�����ԭ�������______��
��4�����磺2CrO42-+2H+
Cr2O72-+H2O
��25��C��KSP��Ag2Cr2O4��=1.12��10-12��KSP��Ag2Cr2O7��=2��10-7����Na2Cr2O7��Һ�м���AgNO3��Һ������ֻ����һ��ש��ɫ�������ó����Ļ�ѧʽ��______��
�ڽ�wg����Na2CrO4��������ˮ���lL��Һ������Һ���й����ӵ�Ũ�ȣ�mol?L-1����pH�Ĺ�ϵ���±���
���ϱ���֪��
��Ҫʹ��Һ��CrO42-�����ﵽ���Ӧ������Һ��pH______���ã�������=��������ݱ�ʾ����
�� w g����Na2CrO4�����ʵ���n=______������ѧ����ʽ��ʾ����
�ο��𰸣���1��Cr���ϼ۴�+6��+3�����ϼ۽���3����Na2CrO4��������������?lmolCr��OH��3ʱת�Ƶ��ӵ����ʵ���Ϊ 3mol��
�ʴ�Ϊ��Na2CrO4 ?3��
��2������״̬ʱ��Cr2O3?�������룺Cr2O3�T2Cr3++3O2-�����Cr2O3��������ӦʽΪ��2O2--4e-�TO2����
�ʴ�Ϊ��2O2--4e-�TO2�� Һ̬��������̬����
��3��������������ϡ���ᡢϡ���ᣬ��������Ũ���ᣬ˵������Ũ�������������ܵı���Ĥ��
�ʴ�Ϊ������������������Ĥ�������ۻ�����
��4������KSP��Ag2Cr2O4��=1.12��10-12��KSP��Ag2Cr2O7��=2��10-7�������ܽ�ƽ�����ܽ��С�����С�ķ���ת����������Na2Cr2O7��Һ�м���AgNO3��Һ������ֻ����һ��ש��ɫ�������ó���Ϊ��Ag2CrO4��
�ʴ�Ϊ��Ag2CrO4��?
?�ڹ۲�������ݿ�֪��PH����c��CrO42-������PH=9ʱ��c��CrO42-��=0.996����Ҫʹ��Һ��CrO42-�����ﵽ���Ӧ������Һ��pH��9��
��Ԫ�ش�����ʽ�У�CrO42-��Cr2O72-��HCrO4-�����������غ�w g����Na2CrO4�����ʵ���Ϊ��n�Tn��CrO42-��+c��Cr2O72-��+n��HCrO4-����
�ʴ�Ϊ����9��n��CrO42-��+c��Cr2O72-��+n��HCrO4-����
���������
�����Ѷȣ�һ��
5��ѡ���� ����ʵ�������ȷ���ǣ�������
A����֤AgI�ܽ�ȱ�AgClС����AgCl����Һ�еμ�KI��Һ
B���к͵ζ�ʵ��ʱ���ô���Һ��ϴ��ƿ
C���ⶨʳ����ҺpHʱ��������ˮ��ʪpH��ֽ
D���ⶨ�к���ʱ������ͨ���������ٽ��跴ӦҺ
�ο��𰸣�A�����ݳ���ת�������������÷�Ӧ������ܵķ�����з�������֤AgI�ܽ�ȱ�AgClС����AgCl����Һ�еμ�KI��Һ��������ɫ�Ӱ�ɫ�仯Ϊ��ɫ��֤���⻯���ܽ��С���Ȼ�������A��ȷ��
B���к͵ζ�ʵ��ʱ���ô���Һ��ϴ��ƿ�����������Һ������������ı�Һ������ʵ���������������жϲ�ý������B����
C��PH��ֽʪ����ٲⶨʳ����ҺPH��ϡ�ʹ�����Һ���ⶨ����ҺPH������C����
D�����β������ڽ���ʱ�������ƶ����裬�����ڲ�������ײ����һ��IJ����������벣������ײ�������������������ʧ����D����
��ѡA��
���������
�����Ѷȣ���