时间:2017-11-11 02:14:40
1、简答题 复印机使用的墨粉主要成份是Fe3O4,如图是氧化沉淀法生产Fe3O4的工艺: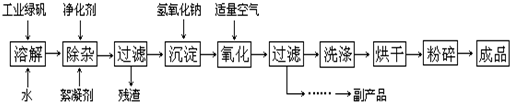
已知:①工业绿矾中FeSO4的含量为52.5%,其中的杂质不参与反应;
②Fe(OH)2+2Fe(OH)3→Fe3O4?4H2O
请回答下列问题:
(1)铁的常见氧化物有______;
(2)Fe3O4与盐酸反应的化学方程式是:______,检验反应后的溶液中含Fe3+的方法:______;
(3)在工艺流程中,通入适量空气“氧化”时的化学方程式是:______;
(4)生产中可获得的副产品是______,提取该副产品的操作顺序是:______(填写序号)
a.过滤?b.加热浓缩?c.冷却?d.结晶?e.洗涤
(5)在生产过程中,若工业绿矾的投料速率是12.16kg/h,为使产品较纯,鼓入空气的速率应为______m3/h(假设反应在标准状态下进行,空气中O2占20%).
2、选择题 Cu、Cu2O和CuO组成的混合物加入100 mL 0.6 mol/L HNO3溶液,恰好使混合物溶解,同时收集到224 mL NO气体(标准状况)。下列说法不正确的是
A.产物中硝酸铜的物质的量为0.025 mol
B.若混合物中Cu的物质的量为0.005 mol,则其中Cu2O、CuO的物质的量共0.020 mol
C.若混合物中含0.01 mol Cu,则其中Cu2O、CuO的物质的量均为0.005 mol
D.混合物中Cu的物质的量的取值范围为0.005 mol<n(Cu)<0.015 mol
3、填空题 (16分)将6.4 g铜加入到50 mL a mol/L的硝酸溶液中,铜全部溶解,得到NO2和NO的混合气体。将反应后溶液稀释至100 mL,测得NO3-的浓度为3 mol/L。试求:
(1)在铜与浓硝酸反应中,硝酸表现出 ;
A.酸性
B.氧化性
C.酸性和氧化性
D.还原性
(2)铜与稀硝酸反应的离子方程式为 ;
(3)反应中生成硝酸铜的物质的量是  mol;
mol;
(4)混合气体中NO2和NO的总物质的量为 m ol(用含a的式子表示);
ol(用含a的式子表示);
(5)稀释后的溶液中H+的物质的量浓度为 mol/L;
(6)若a=9,则混合气体中NO2的质量为 g;
(7)用NaOH溶液吸收产生的混合气体,原理为:
2NO2+2NaOH=NaNO2+NaNO3+H2O; NO2+NO+2NaOH= 2NaNO2+H2O
2NaNO2+H2O
若生成的混合气体能被NaOH溶液完全吸收,则a的取值范围为 。
4、选择题 下列叙述I和II均正确并且有因果关系的是
| 选项 | 陈述I | 陈述II |
| A | NH4Cl为强酸弱碱盐 | 用加热法除去NaCl中的NH4Cl |
| B | Fe3+具有氧化性 | 用KSCN溶液可以鉴别Fe3+ |
| C | 溶解度:CaCO3<Ca(HCO3)2 | 溶解度:Na2CO3<NaHCO3 |
| D | SiO2可与HF反应 | 氢氟酸不能保存在玻璃瓶中 5、填空题 如图,盛有足量水的水槽里放两个烧杯,小烧杯里放有少量铜片和过量浓硝酸,小烧杯外面倒扣一个大烧杯,请回答: |