时间:2017-11-11 01:56:54
1、填空题 (13分)已知NaHSO3溶液显酸性,而Na2SO3溶液显碱性。
(1)25℃时,在20.0mL0.5mol・L-1的NaOH溶液中,通入标准状态下的224mLSO2,所得溶液显______(填“酸”或“碱”)性,原因是_______________________________(用?化学用语表达),溶液中所含有的离子浓度由大到小的顺序为____________________。
(2)在上述溶液中逐滴加入1mol・L-1NaClO溶液至20mL,反应的离子方程式为____________________。当滴加NaClO至10mL时,溶液中由水电离的H+离子浓度为______________mol・L-1。滴加至20mL时溶液中离子浓度由大到小的顺序为_________________________。
(3)若在(2)反应后的溶液中滴加少量甲基橙,溶液显_________色。
参考答案:(1)酸(1分)? HSO3- H++SO32-?c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-)
H++SO32-?c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-)
(2)HSO3-+ClO-=SO42-+Cl-+H+? 3×10-14? c(Na+)>c(SO42-)=c(Cl-)>c(H+)>c(ClO-)>c(OH-)?(3)无?(其余每空2分)
本题解析:略
本题难度:简单
2、填空题 在氯化铁溶液中存在平衡:FeCl3+3H2O Fe(OH)3+3HCl △H>0。
Fe(OH)3+3HCl △H>0。
(1)加热FeCl3溶液,溶液的颜色会加深,可得到一种红褐色透明液体,向这种液体里加入MgCl2溶液,产生的现象为________。
(2)在配制FeCl3溶液时,为防止浑浊,应加入_______。
参考答案:生成红褐色沉淀;少许浓盐酸。
本题解析:(1)FeCl3+3H2O Fe(OH)3+3HCl △H>0该反应为吸热反应,加热FeCl3溶液,使水解平衡正向移动,得到红褐色透明液体是Fe(OH)3胶体,根据胶体的性质,加入电解质会使胶体聚沉。故答案为生成红褐色沉淀。(2)FeCl3+3H2O
Fe(OH)3+3HCl △H>0该反应为吸热反应,加热FeCl3溶液,使水解平衡正向移动,得到红褐色透明液体是Fe(OH)3胶体,根据胶体的性质,加入电解质会使胶体聚沉。故答案为生成红褐色沉淀。(2)FeCl3+3H2O Fe(OH)3+3HCl,为防止浑浊,就要控制Fe(OH)3的产生,即需要抑制水解。增大H+的浓度,能有效抑制水解。故答案为加入少量浓盐酸。
Fe(OH)3+3HCl,为防止浑浊,就要控制Fe(OH)3的产生,即需要抑制水解。增大H+的浓度,能有效抑制水解。故答案为加入少量浓盐酸。
点评:理解影响水解平衡的因素,并能理解胶体的制备。
本题难度:一般
3、选择题 二元酸H2A在水中发生电离:H2A=H++HA-和HA-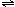 H++A2-,则下列几种物质的水溶液中关系式不正确的是
H++A2-,则下列几种物质的水溶液中关系式不正确的是
A.NaHA:c(Na+)>c(HA-)>c(OH-)>c(H+)
B.NaHA:c(Na+)=c(A2-)+c(HA-)
C.Na2A:c(Na+)>c(A2-) >c(OH-)>c(H+)
D.H2A:c(H+)=c(HA-)+2 c(A2-)+c(OH-)
参考答案:A
本题解析:根据电离方程式可知,该酸的第一步是完全电离的,而第二步是不完全的,存在电离平衡。所以HA-只能电离,而不能水解,溶液是显酸性的,A不正确。根据原子守恒可知,B是正确的。Na2A水解显碱性,C正确。根据电荷守恒中D也是正确的。答案选A。
本题难度:一般
4、选择题 把AlCl3溶液蒸干灼烧,最后得 到的固体产物是?
到的固体产物是?
A.AlCl3・6H2O
B.AlCl3
C.Al(OH)3
D.Al2O3
参考答案:D
本题解析:略
本题难度:简单
5、选择题 Fe(NO3)2溶液呈浅绿色,其中存在下列平衡:Fe2+ +2H2O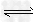 Fe(OH)2+2H+,往该溶液中逐滴加入盐酸,发生的变化是?
Fe(OH)2+2H+,往该溶液中逐滴加入盐酸,发生的变化是?
[? ]
A、因为增大了H+的浓度,导致平衡逆移,所以Fe2+的浓度增大 ?
B、平衡正向移动?
C、溶液颜色由浅绿色变黄色?
D、生成红褐色沉淀
参考答案:C
本题解析:
本题难度:一般