时间:2017-11-11 01:46:55
1、选择题 下列比值为2∶1的是
A.pH=2与pH=1的硝酸中c(H+)之比
B.Na2CO3溶液中c(Na+)与c(CO32ˉ )之比
C.0.2mol/L与0.1mol/L醋酸中c(H+)之比
D.NO2溶于水时,被氧化的n(NO2)与被还原的n(NO2)之比为
参考答案:D
本题解析:pH=2与pH=1的硝酸中c(H+)分别为0.01mol·L-1和0.1 mol·L-1,因此c(H+)之比为1︰10,A不正确。Na2CO3溶液中CO32ˉ要水解,使其浓度减小,所以c(Na+)与c(CO32ˉ )之比应大于2∶1,B不正确;醋酸属于弱酸,存在电离平衡,因此若将0.2mol/L醋酸稀释到0.1mol/L,溶液中的c(H+)应大于原来的十分之一,即0.2mol/L与0.1mol/L醋酸中c(H+)之比应小于10︰1,C不正确;NO2溶于水的反应式为3NO2+H2O=2HNO3+NO,所以被氧化的n(NO2)与被还原的n(NO2)之比为2︰1,D正确。答案选D
本题难度:简单
2、填空题 (6分)某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂。请填写下列空白:
(1)终点的判断:溶液由_____________________________________________________。
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是(? )
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用
盐酸溶液的体积为_________ml。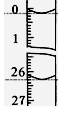
(4)某学生根据3次实验分别记录有关数据如表:
| 滴定 次数 | 待测NaOH溶液的体积/mL | 0.1000 mol/L盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 平均耗用盐酸 体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.15 | ①V=__________ |
| 第二次 | 25.00 | 0.56 | 30.30 | |
| 第三次 | 25.00 | 0.20 | 26.45 | |
参考答案:(1)浅红色变为无色且半分钟内不恢复 (2)D ? (3) 26.10
(4)V=26.20 ml,(第二次偏差太大,舍去)
c(NaOH)=0.1000 mol/L×26.20 mL/25.00 mL=0.1048 mol/L
本题解析:略
本题难度:一般
3、选择题 下列有关电解质溶液关系正确的是
A.分别向pH=2的盐酸和醋酸溶液中,加水稀释到pH=4,消耗水的体积相等
B.等物质的量浓度的氯化钠和醋酸钠溶液中,微粒关系有c(Na+)= c(Cl-)+c(CH3COO-)
C.在NaHSO3溶液微粒由大到小的顺序为:c(Na+)>c(HSO3-)>c(SO32-)>c(H2SO3)
D.若弱酸的酸性H2A>H2B,则等物质的量浓度等体积的Na2A、Na2B溶液中,阴离子数目前者大于后者
参考答案:C
本题解析:选项A中盐酸为强酸,醋酸为弱酸,加水稀释时醋酸消耗水的体积大。选项B中油正负电荷守恒得c(Na+)+c(H+)= c(Cl-)+c(CH3COO-)。选项D中H2A酸性强于H2B,B2-离子与氢离子结合的能力强于A2-离子,因此Na2A的碱性弱于Na2B。再根据c(Na+)+c(H+)=c(A2-)+c(OH-) ,
c(Na+)+c(H+)=c(A2-)+c(OH-),Na+浓度相同,A中的c(H+)大于B中c(H+),可得Na2A溶液中的阴离子数多
点评:本题关键在于会利用物料守恒,及溶液的性质来判断离子浓度的大小。
本题难度:简单
4、选择题 以甲基橙为指示剂,用0.10 mol·L-1的盐酸滴定0.10 mol·L-1的氨水,
滴定过程中不可能出现的结果是(?)
A.c(NH4+)>c(Cl-),c(OH-)>c(H+)
B.c(NH4+)=c(Cl-),c(OH-)=c(H+)
C.c(Cl-)>c(NH4+),c(OH-)>c(H+)
D.c(Cl-)>c(NH4+),c(H+)>c(OH-)
参考答案:C
本题解析:解答本题时要注意两点:
(1)明确指示剂的变色范围;
(2)根据指示剂的变色范围判断滴定过程中溶液酸碱性的变化。
本题难度:一般
5、选择题 下列说法正确的是
A.在铁船闸上装若干铜块以减缓其腐蚀
B.Zn具有还原性和导电性,可用作锌锰干电池的负极材料
C.电解精炼铜时,阳极质量每减少32g,阴极析出的铜质量也为32g
D.钢铁发生吸氧腐蚀时,Fe作负极,负极反应式为:Fe-3e-=Fe3+
参考答案:B
本题解析:A.在铁船闸上装若干锌块以减缓其腐蚀;
C.电镀时,阳极质量每减少32g,阴极析出的铜质量也为32g;
D.钢铁发生吸氧腐蚀时,Fe作负极,负极反应式为:Fe-2e-=Fe2+。
故选B。
点评:此题要求学生能熟练掌握电化学的基本知识,如金属的防护,电解池,电镀池,原电池的知识。只要熟悉,此题便不难解决。
本题难度:简单