时间:2017-11-05 23:33:42
1、选择题 下列叙述正确的是
A.在pH=1的溶液中,Cu2+、Fe2+、NO3-和SO42-能大量共存
B.用惰性电极电解饱和氯化钠溶液的离子方程式:2Cl- + 2H+ = H2↑+ Cl2↑
C.镁铝合金被碱液腐蚀时,负极反应式为:Mg — 2e- = Mg2+
D.大量使用含磷洗涤剂会造成水体富营养化
参考答案:D
本题解析:A.pH=1的溶液显酸性,则Fe2+与NO3-发生氧化还原反应,不能大量共存,A错误;B.用惰性电极电解饱和氯化钠溶液的离子方程式为:2Cl- + 2H2O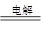 H2↑+ Cl2↑+2OH—,B错误;C.镁铝合金被碱液腐蚀时,铝与碱液反应,则负极反应式为:Al — 3e- +4OH—=AlO2—+2H2O,C错误;D.磷元素是植物生长的必需元素,因此大量使用含磷洗涤剂会造成水体富营养化,D正确,答案选D。
H2↑+ Cl2↑+2OH—,B错误;C.镁铝合金被碱液腐蚀时,铝与碱液反应,则负极反应式为:Al — 3e- +4OH—=AlO2—+2H2O,C错误;D.磷元素是植物生长的必需元素,因此大量使用含磷洗涤剂会造成水体富营养化,D正确,答案选D。
考点:考查离子共存、电化学原理以及水体富营养化
本题难度:一般
2、选择题 下列描述中,不符合生产实际的是( )
A.合成氨工业中,N2和H2的最佳配比应为物质的量之比1:3
B.电解法精炼粗铜,用纯铜作阴极
C.工业上电解饱和食盐水制烧碱,用离子交换膜阻止0H-移向阳极
D.在镀件上电镀锌,锌作阳极
参考答案:A、合成氨工业中,氮气比较廉价,为了提高氢气的转化率要加入过量的氮气,所以N2和H2的物质的量之比大于1:3,故A错误.
B、电镀时,镀层作阳极,镀件作阴极,所以纯铜作阴极,粗铜作阳极,故B正确.
C、工业上电解饱和食盐水制烧碱,溶液中阴离子向阳极移动,阳离子向阴极移动,用离子交换膜阻止0H-移向阳极,故C正确.
D、电镀时,镀层作阳极,镀件作阴极,镀层为锌,所以锌作阳极,故D正确.
故选A.
本题解析:
本题难度:简单
3、选择题 pH=a的某电解质溶液中,插入两支石墨电极通直流电一段时间后,溶液的pH>a,则该电解质可能是
[? ]
A. NaOH
B. H2SO4
C. AgNO3
D. Na2SO4
参考答案:A
本题解析:
本题难度:一般
4、选择题 烧碱的制备,在上世纪七十年代常用水银法,此法通过钠汞齐(Na·nHg)生产得到的烧碱质量好,浓度高,目前已被离子交换膜法所取代。两种生产方法示意图如下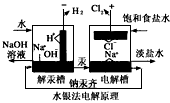

下列说法正确的是
[? ]
A.水银法被淘汰,是因为生产过程中,汞不能循环利用
B.水银法生产,在电解槽中,阴极的电极反应式为:Na++e-+nHg=Na·nHg
C.离子膜法电解,阳极发生的电极反应为:2H++2e-=H2↑
D.水银法中烧碱在电解槽中生成,离子膜法烧碱在阴极生成
参考答案:B
本题解析:
本题难度:一般
5、选择题 下图是电解CuCl2溶液的装置,其中c、d为石墨电极。则下列有关的判断正确的是
A.电解过程中,d电极质量增加
B.d为阳极,电极反应为:2Cl? - 2e- = Cl2↑
C.a为负极、b为正极
D.电解过程中,氯离子浓度不变
参考答案:A
本题解析:从电流的流向可以判断a是正极,b是负极,A.电解过程中,d电极接电源的负极做阴极,发生反应为:Cu2+ + 2e- =Cu,质量增加,对;B.d电极接电源的负极做阴极,不是阳极,错;C.a为正极、b为负极,错;D.电解过程中,氯离子在阳极放电,发生2Cl? - 2e- = Cl2↑浓度减小,错,选A。
考点:电解池的工作原理。
本题难度:一般