时间:2017-11-05 22:40:25
1、选择题 蝇类昆虫的雌性信息素可用芥酸(来自白芥)与羧酸X在浓NaOH溶液中进行阳极氧化得到.电解总反应式为C21H41COOH+X+4NaOH→C23H46+2Na2CO3+2H2O+H2,则下列说法正确的是( )
A.X为C2H5COOH
B.电解的阳极反应式为:C21H41COOH+X-2e-+2H2O→C23H46+2CO32-+6H+
C.电解过程中,每转移2mol电子,则生成2mol雌性信息素
D.阴极的还原产物为H2和OH-
参考答案:A
本题解析:
本题难度:一般
2、简答题 Zn-MnO2干电池应用广泛,其示意图如下,电解质溶液是ZnCl2-NH4Cl混合溶液.
(1)该电池的负极材料是______.电池工作时,电子流向______(填“正极”或“负极”).
(2)如果该电池的工作原理为:Zn+2NH4Cl=ZnCl2+2NH3+H2,其正极反应式为:______
(3)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀.其主要原因是______.欲除去Cu2+,最好选用下列试剂中的______(填代号).
a.NaOHb.Zn c.Fed.NH3?H2O
(4)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液.阴极的电极反应式是:______;若电解电路中通过2mol电子,MnO2的理论产量为______.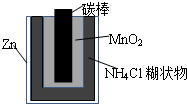
参考答案:(1)负极上是失电子的,则Zn失电子为负极,电子由负极流向正极,
故答案为:Zn(或锌);正极;
(2)正极上是阳离子的电子发生还原反应的过程,该反应为2NH4++2e-=2NH3+H2,
故答案为:2NH4++2e-=2NH3+H2;
(3)电化学腐蚀较化学腐蚀更快,锌与还原出来的Cu构成铜锌原电池而加快锌的腐蚀.题目中a和d选项不能除去杂质离子,c项会引入新杂质,所以应选Zn将Cu2+置换为单质而除去,
故答案为:锌置换出铜,Zn+Cu2+=Cu+Zn2+,在溶液中,构成铜锌原电池,加快化学反应速率;b;
(4)阴极上得电子,发生还原反应,H+得电子生成氢气,因为MnSO4~MnO2~2e-,通过2mol电子产生1molMnO2,其质量为87g,
故答案为:2H++2e-→H2;87g.
本题解析:
本题难度:一般
3、实验题 (1)(19分)①研究性学习小组为了证明铁的金属性比铜强,他设计了如下几种方案,其中合理的是 (填序号)
A.铁片置于硫酸铜溶液中有铜析出;
B.铁、铜与氯气反应分别生成FeCl3、CuCl2;
C.铜片置于FeCl3溶液中,铜片逐渐溶解(2FeCl3+Cu=2FeCl2+ CuCl2)
D.铁片、铜片分别置于盛有稀硫酸的烧杯中,铁片上有气泡产生,而铜片无气泡
E.常温下,分别将铁片和铜片置于浓硝酸中,铁片不溶解,而铜片溶解
②请你另设计一个能证明铁的金属活动性比铜强的实验。要求:
a.此方案的原理不同于上述任一合理方案;
b.在方框内绘出实验装置图并注明所需的药品;
c.写出实验过程中的主要实验现象并用相关化学用语解释现象
(2)学完原电池的相关知识后,甲组同学认为构成原电池必须有三个条件:①活动性不同的两极;②电解质溶液;③闭合回路。乙组同学对条件①提出异议,认为相同的两极也可以构成原电池,以下为乙组同学的实验装置简图以及实验报告的部分内容。请仔细阅读实验报告,然后将实验报告补充完整并填在相应的横线上。装置中盐桥的作用之一是使整个装置构成闭合回路。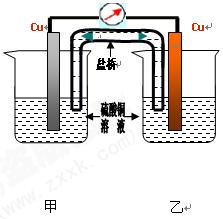
浓差电池与温差电池
一、【实验目的】
1、电池中两杯溶液及电极均相同,两杯溶液的浓度不同,可否形成原电池
2、电池中两杯溶液 及电极均相同,两杯溶液的温度不同,可否形成原电池
及电极均相同,两杯溶液的温度不同,可否形成原电池
3、电池中两杯溶液及电极均相同,研究两杯溶液的 对电池电压和电流的影响
4、电池中两杯溶液及电极均相同,研究两杯溶液的 对电池电压和电流的影响
二、【仪器与药品】略。
三、【实验方法与步骤】
Ⅰ、实验方法:略。
Ⅱ、研究的步骤
㈠实验A:浓差电池
电解液均为硫酸铜,电极均为铜片:
1、甲烧杯中固定装入浓度 0.8 mol/L 的硫酸铜溶液。
2、乙烧杯中分
参考答案:
本题解析:
本题难度:一般
4、填空题 某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的开关K时,观察到电流计的指针发生了偏转。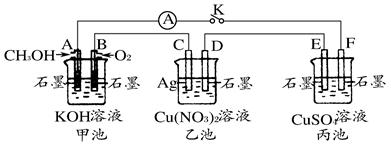
请回答下列问题:
(1)甲、乙、丙三池中为原电池的是__________(填“甲池”、“乙池”或“丙池”)。
(2)丙池中F电极为__________(填“正极”、“负极”、“阴极”或“阳极”),该池的总反应式为__________。
(3)当乙池中C电极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为__________mL(标准状况)。
(4)一段时间后,断开开关K。下列物质能使丙池恢复到反应前浓度的是__________(填选项字母)。
A.Cu
B.CuO
C.CuCO3
D.Cu2(OH)2CO3
参考答案:(1)甲池 (2)阴极 2CuSO4+2H2O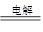 2H2SO4+2Cu+O2↑ (3)560 (4)BC
2H2SO4+2Cu+O2↑ (3)560 (4)BC
本题解析:(1)甲、乙、丙三池中只有甲池中的氧化还原反应能自发进行,因此甲池为原电池。(2)丙池中F电极与甲池负极相连,为阴极,丙池为电解硫酸铜溶液,总反应式为2CuSO4+2H2O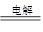 2H2SO4+2Cu+O2↑。(3)乙池中C电极反应式为Ag-e-=Ag+,甲池中B电极反应式为2H2O+O2+4e-=4OH-,则有关系式:4Ag~O2,故V(O2)=
2H2SO4+2Cu+O2↑。(3)乙池中C电极反应式为Ag-e-=Ag+,甲池中B电极反应式为2H2O+O2+4e-=4OH-,则有关系式:4Ag~O2,故V(O2)=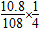 ×22.4=0.56 L。(4)从丙池的电解总反应式可以看出,溶液中减少的“2Cu+O2”相当于CuO,因此可以加入CuO或CuCO3。
×22.4=0.56 L。(4)从丙池的电解总反应式可以看出,溶液中减少的“2Cu+O2”相当于CuO,因此可以加入CuO或CuCO3。
本题难度:一般
5、实验题 (7分)将质量相等的锌片和铜片用导线相连浸入500mL硫酸铜溶液中构成如下图的装置。
(1)此装置为?_______________,该装置中发生反应总的离子方程式为?_______________,铜片周围溶液会出现?_______________的现象。
(2)若2 min后测得锌片质量减少1.3g,则导线中流过的电子为_______________mo1。
(3)该装置的电解质溶液还可以用? _______________(答一种即可)。
参考答案:(7分)
(1)原电池(1分)? Zn+Cu2+="===Zn2++Cu" (2分)?颜色变浅(1分)
(2)0.04 (2分)?
(3)稀硫酸(或其他合理的酸、盐等)(1分)
本题解析:略
本题难度:简单