时间:2017-11-05 22:16:34
1、选择题 为证明某可溶性一元酸(HX)是弱酸,有如下实验方案,其中不合理的是
A.室温下,测0.1 mol/L HX溶液的pH,若pH>1,证明HX是弱酸
B.室温下,测1 mol/L NaX溶液的pH,若pH>7,证明HX是弱酸
C.将等浓度、等体积的HCl和NaX溶液混合,若混合溶液pH<7,证明HX是弱酸
D.相同条件下,对0.1 mol/L的HCl和0.1 mol/L的HX进行导电性实验,若与HX溶液相串联的灯泡较暗,证明HX为弱酸
参考答案:C
本题解析:试题分析:A.若是弱酸,电离出的氢离子浓度小于0.1mol/L,因来源:91考试网 91Exam.org此PH>1,正确
B.若HX是弱酸,那么NaX就是强碱弱酸盐,水溶液呈碱性,正确
C.想利用强制弱原理,但是假如HX是强酸的话,这个反应不会发生,但是因为里面有盐酸,因此溶液依旧会显酸性。D.等浓度的两种酸在相同条件测导电性,实际是测溶液中电离产生的阴阳离子的浓度,离子浓度越小,导电性越弱。正确
考点:酸的电离
点评:本题考查弱酸的电离及其应用
本题难度:一般
2、选择题 下列说法正确的是( )
A.水溶液显碱性的都属于碱
B.盐溶液不一定都呈中性
C.凡能电离出H+的化合物均属于酸
D.盐类物质一定含有金属阳离子
参考答案:B
本题解析:
本题难度:简单
3、选择题 在下列叙述中,不能说明醋酸是弱电解质的是(? )
A.室温下,0.1mol・L-1的CH3COONa溶液的pH=8
B.室温下,0.1mol・L-1的CH3COOH溶液的pH="3"
C.醋酸中加水后,溶液的pH升高
D.0.1mol・L-1的CH3COOH导电能力不如0.1mol・L-1的盐酸强
参考答案:C
本题解析:A可以,如果醋酸是强电解质强酸,那么醋酸根离子就不会水解,使溶液呈碱性。
B可以,醋酸是强酸强电解质,那么0.1mol・L-1的CH3COOH溶液的pH=1
C不能,对任何酸加水稀释都会使PH升高。
D可以,同浓度的情况下两种一元酸进行比较,直接可以说明醋酸中离子浓度比强电解质盐酸中的少,可以说明其是弱电解质。
本题难度:一般
4、选择题 根据要求填空:
(1)在0.1mol/L的CH3COOH溶液中,若加入少量的蒸馏水,溶液的pH ;若加入少量的纯醋酸,溶液中的c(CH3COO―) ;若加入少量的NaOH固体,溶液中的c(H+) ;若加入少量的CH3COONa固体,溶液中的c(OH―) 。(以上均用“增大”、“减小”或“不变”填空)
(2)在以KOH为电解质溶液的氢氧燃料电池中,电池工作时其负极的电极反应式为 正极的电极反应式为 。
参考答案:(1)增大;增大;减小;增大。(2)2H2-4e―+4OH―=4H2O , O2+4e―+2H2O=4OH―
本题解析:(1)对于0.1mol/L的稀CH3COOH溶液中,若加入少量的蒸馏水,电离平衡CH3COOH  CH3COO-+H+.向正反应方向移动,使溶液的H+浓度增大,但水对离子的稀释作用大于平衡正向移动使离子浓度增大的趋势,总的来说C(H+)减小,所以溶液的pH增大。若加入少量的纯醋酸,由于C(CH3COOH)增大,平衡正向移动,使C(CH3COOH)减小,溶液中的c(CH3COO―)增大。若加入少量的NaOH固体,由于发生反应:H++OH-=H2O消耗了溶液中的H+,使c(H+)减小,平衡正向移动使c(H+)又有所增加,但消耗的浓度大于平衡增加的浓度,总的来说溶液中c(H+)减小。若加入少量的CH3COONa固体,溶液中的c(CH3COO―)增大,平衡逆向移动,溶液中c(H+)减小,c(OH―)增大。(2)以KOH为电解质溶液的氢氧燃料电池中,通入H2的电极为负极,电池工作时其负极的电极反应式为2H2-4e―+4OH―=4H2O,通入O2的电极为正极,正极的电极反应式为O2+4e―+2H2O=4OH―。总反应式为2H2+O2=2H2O。
CH3COO-+H+.向正反应方向移动,使溶液的H+浓度增大,但水对离子的稀释作用大于平衡正向移动使离子浓度增大的趋势,总的来说C(H+)减小,所以溶液的pH增大。若加入少量的纯醋酸,由于C(CH3COOH)增大,平衡正向移动,使C(CH3COOH)减小,溶液中的c(CH3COO―)增大。若加入少量的NaOH固体,由于发生反应:H++OH-=H2O消耗了溶液中的H+,使c(H+)减小,平衡正向移动使c(H+)又有所增加,但消耗的浓度大于平衡增加的浓度,总的来说溶液中c(H+)减小。若加入少量的CH3COONa固体,溶液中的c(CH3COO―)增大,平衡逆向移动,溶液中c(H+)减小,c(OH―)增大。(2)以KOH为电解质溶液的氢氧燃料电池中,通入H2的电极为负极,电池工作时其负极的电极反应式为2H2-4e―+4OH―=4H2O,通入O2的电极为正极,正极的电极反应式为O2+4e―+2H2O=4OH―。总反应式为2H2+O2=2H2O。
考点:考查燃料电池电极式的书写及外界条件对弱电解质电离平衡、离子浓度溶液酸碱性的影响的知识。
本题难度:一般
5、实验题 某学生在0.1mol/LNaHCO3溶液中滴加酚酞溶液1滴,整个溶液几乎没有什么变化,但溶液加热后,显明显淡红色,加热较长时间后冷却,红色不褪去。
该学生为了了解该过程的原因,进行了下列探究过程:
【实验探究】
实验1: 加热0.1mol/LNaHCO3溶液,测得溶液pH变化如下表
| 温度(℃) | 10 | 20 | 30 | 50 | 70 | 80 | 100 |
| pH | 8.3 | 8.4 | 8.5 | 8.9 | 9.4 | 9.6 | 10.1 |
参考答案:(本题共12分,每空1分)
(1)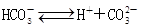 、
、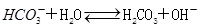 水解平衡,溶液显碱性
水解平衡,溶液显碱性
(2)加热0.1mol/LNaHCO3溶液,NaHCO3发生分解反应或促进水解平衡,产生二氧化碳。
(3)水分蒸发,NaHCO3发生分解反应,NaHCO3水解平衡被促进
(4)相同温度下,Na2CO3的水解能力和溶液碱性大于NaHCO3
(5)排除因水分蒸发导致pH增大的因素。NaHCO3常温下即可发生分解反应或碳酸氢钠水解平衡和二氧化碳溶解平衡移动。
(6)是NaHCO3发生分解生成碳酸钠?还是水解平衡向右移动?还是两者皆有。(相关合理答案均可得分)
本题解析:(1)NaHCO3为弱酸酸式盐,可发生电离,也发生水解反应,根据实验1表中数据可知NaHCO3溶液呈碱性,所以以水解为主。
(2)加热0.1mol/LNaHCO3溶液,将产生的气体通入澄清石灰水,溶液变浑浊,说明生成的气体为CO2。
(3)实验2温度升高,溶液的pH增大,说明加热促进了NaHCO3的水解,实验三生成了CO2,可能为NaHCO3发生了分解反应。
(4)Na2CO3溶液的pH大,说明Na2CO3溶液的碱性强,水解程度大。
(5)加水至200mL,与原溶液体积相同,排除因水分蒸发而导致pH增大;常温下溶液的pH增大,可能是NaHCO3在常温下分解,也可能是NaHCO3的水解程度增大,或CO2的溶解平衡移动造成的后果。
(6)NaHCO3溶液加热后pH增大,可能为NaHCO3发生分解生成碳酸钠,也可能是NaHCO3水解平衡向右移动,或者两种都有,需要进一步研究。
本题难度:困难