时间:2017-11-05 20:47:13
1、填空题 现有常温下的0.1 mol/l纯碱溶液。
(1)该溶液呈碱性是因为存在水解平衡,相关离子方程式是:________________。为证明存在上述平衡,进行如下实验:在0.1 mol・l-1纯碱溶液中滴加酚酞,溶液显红色,再往溶液中滴加?(填化学式)溶液,红色逐渐退为无色,说明上述观点成立。
(2)同学甲查阅资料得知0.1 mol/LNa2CO3中,发生水解的CO32―不超过其总量的10%。请设计实验加以证明(写出实验方案及预期观察到的现象)。答:?。
(3)同学乙就该溶液中粒子浓度关系写出五个关系式,其中不正确的是?。
A.c(Na+)>2c(CO32―)
B.c(CO32―)>c(OH-)>c(HCO3―)>c(H2CO3)
C.c(OH-)=c(H+)+c(HCO3―)+2c(H2CO3)
D.c(CO32―)+c(HCO3―)="0.1" mol・L-1
E.c(H+)+ c(Na+)= c(OH-)+c(HCO3―)+c(CO32―)
(4)室温下pH均为a的Na2CO3和NaOH溶液中,水电离产生的c(OH―)之比=?。
参考答案:(1)CO32- + H2O HCO3- + OH-? BaCl2或CaCl2
HCO3- + OH-? BaCl2或CaCl2
(2)测0.1 mol・L-1Na2CO3溶液pH,pH≤12?(3)D、E?(4)10(2a-14)
本题解析:(1) 纯碱碳酸钠是强碱弱酸盐。在溶液中存在的水解平衡主要是CO32- + H2O HCO3- + OH-,还有HCO3- + H2O
HCO3- + OH-,还有HCO3- + H2O H2CO3-+ OH-。由于消耗了水电离产生的H+,所以最终使溶液中的c(OH-)>c(H+)。因此溶液显碱性。再往溶液中滴加与CO32-形成沉淀的物质如BaCl2或CaCl2,此时会放出沉淀反应,消耗了CO32-,c(CO32-)减小,尽管水解程度增大,但是单位体积中的OH-的物质的量减少,所以溶液的碱性减弱,红色逐渐退为无色。(2)在Na2CO3溶液中主要存在水解平衡CO32- + H2O
H2CO3-+ OH-。由于消耗了水电离产生的H+,所以最终使溶液中的c(OH-)>c(H+)。因此溶液显碱性。再往溶液中滴加与CO32-形成沉淀的物质如BaCl2或CaCl2,此时会放出沉淀反应,消耗了CO32-,c(CO32-)减小,尽管水解程度增大,但是单位体积中的OH-的物质的量减少,所以溶液的碱性减弱,红色逐渐退为无色。(2)在Na2CO3溶液中主要存在水解平衡CO32- + H2O HCO3- + OH-。c(CO32-)(始)=" 0.1" mol/L,若其水解程度等于10%,根据水解方程式可知:c(OH-)=0.01mol/L.c(H+)=10-12mol/L.pH=12.水解程度越大,水解产生的c(OH-)就越高,溶液的pH就越大。若水解程度小于10%,则c(H+)>10-12mol/L.pH<12.因此,测0.1 mol・L-1Na2CO3溶液pH,若pH≤12就证明0.1 mol/LNa2CO3中,发生水解的CO32―不超过其总量的10%。(3)A根据物料守恒可得c(Na+)=2c(CO32―)+2 c(HCO3―)+2c(H2CO3).所以c(Na+)>2c(CO32―) 。正确。B.在Na2CO3中存在水解平衡:CO32- + H2O
HCO3- + OH-。c(CO32-)(始)=" 0.1" mol/L,若其水解程度等于10%,根据水解方程式可知:c(OH-)=0.01mol/L.c(H+)=10-12mol/L.pH=12.水解程度越大,水解产生的c(OH-)就越高,溶液的pH就越大。若水解程度小于10%,则c(H+)>10-12mol/L.pH<12.因此,测0.1 mol・L-1Na2CO3溶液pH,若pH≤12就证明0.1 mol/LNa2CO3中,发生水解的CO32―不超过其总量的10%。(3)A根据物料守恒可得c(Na+)=2c(CO32―)+2 c(HCO3―)+2c(H2CO3).所以c(Na+)>2c(CO32―) 。正确。B.在Na2CO3中存在水解平衡:CO32- + H2O HCO3- + OH-, HCO3- + H2O
HCO3- + OH-, HCO3- + H2O H2CO3-+ OH-。主要是第一步水解,所以c(HCO3―)> c(H2CO3);但是盐水解的程度是很微弱的,盐的电离作用大于水解作用,所以c(CO32―)> >c(HCO3―)。由于两步水解都产生OH-,HCO3―第一步水解产生,而在第二步水解中由消耗。所以c(OH-)>c(HCO3―)。因此在溶液中离子间的关系为: c(CO32―)>c(OH-)>c(HCO3―)>c(H2CO3)。正确。C.溶液显碱性。根据质子守恒可得:c(OH-)=c(H+)+c(HCO3―)+2c(H2CO3)。正确。D.根据物料守恒可得c(CO32―)+c(HCO3―)+ c(H2CO3)="0.1" mol/L.错误。E.根据电荷守恒可得c(H+)+ c(Na+)= c(OH-)+c(HCO3―)+2c(CO32―).错误。(4)室温下pH均为a的Na2CO3溶液,c(H+)=10-a, c(OH-)(水)=10-14÷10-a =10a-14mol/L.对于pH=a的NaOH溶液c(H+)(水)= c(OH-)(水)=10-amol/L.所以水电离产生的c(OH―)之比=10a-14:10-a=10(2a-14)。
H2CO3-+ OH-。主要是第一步水解,所以c(HCO3―)> c(H2CO3);但是盐水解的程度是很微弱的,盐的电离作用大于水解作用,所以c(CO32―)> >c(HCO3―)。由于两步水解都产生OH-,HCO3―第一步水解产生,而在第二步水解中由消耗。所以c(OH-)>c(HCO3―)。因此在溶液中离子间的关系为: c(CO32―)>c(OH-)>c(HCO3―)>c(H2CO3)。正确。C.溶液显碱性。根据质子守恒可得:c(OH-)=c(H+)+c(HCO3―)+2c(H2CO3)。正确。D.根据物料守恒可得c(CO32―)+c(HCO3―)+ c(H2CO3)="0.1" mol/L.错误。E.根据电荷守恒可得c(H+)+ c(Na+)= c(OH-)+c(HCO3―)+2c(CO32―).错误。(4)室温下pH均为a的Na2CO3溶液,c(H+)=10-a, c(OH-)(水)=10-14÷10-a =10a-14mol/L.对于pH=a的NaOH溶液c(H+)(水)= c(OH-)(水)=10-amol/L.所以水电离产生的c(OH―)之比=10a-14:10-a=10(2a-14)。
本题难度:一般
2、填空题 中学化学实验中,淡黄色的pH试纸常用于测定溶液的酸碱性。在25 ℃时,若溶液的pH=7,试纸不变色;若pH<7,试纸变红色;若pH>7,试纸变蓝色。而要精确测定溶液的pH,需用pH计。pH计主要通过测定溶液中H+浓度来测定溶液的pH。
(1)已知水中存在平衡:H2O H++OH- ΔH>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是?(填字母)。
H++OH- ΔH>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是?(填字母)。
A.向水中加入NaHSO4
B.向水中加入Cu(NO3)2
C.加热水至100 ℃[其中c(H+)=1×10-6 mol・L-1]
D.在水中加入(NH4)2SO4
(2)现欲测定100 ℃沸水的pH及酸碱性,若用pH试纸测定,则试纸显?色,溶液呈?性(填“酸”、“碱”或“中”);若用pH计测定,则pH?7(填“>”、“<”或“=”),溶液呈?性(填“酸”、“碱”或“中”)。
参考答案:(1)BD (2)淡黄 中 < 中
本题解析:(1)要使平衡右移,且所得溶液呈酸性,应减少OH-的量,所以选B、D。(2)100 ℃时,pH=6溶液呈中性,因此用pH计测定时,pH应小于7,因为溶液是中性,所以pH试纸呈淡黄色。
本题难度:一般
3、填空题 (7分)(1)室温下,把1 mL 0.1 mol・L-1的H2SO4加水稀释成2 L溶液,在此溶液中由水电离产生的H+,其浓度接近于?
(2)室温时,将0.1 mol/L盐酸和0.07mol/L氢氧化钡溶液1:5(体积比)混合后,该混合溶液的pH=_______
(3)某温度时,0.1 mol・L-1NaOH溶液的pH=12。该温度下,10体积pH=a的某强酸与1体积pH=b的某强碱混合后,溶液呈中性,则a和b满足的关系____________________
参考答案: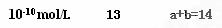
本题解析:略
本题难度:一般
4、选择题 将纯水加热至80℃,下列叙述正确的是(?)?
A.水的离子积不变
B.水的pH变小,呈酸性
C.水的pH变大,呈中性
D.水中的c(H+)=c(OH-)>1×10-7 mol/L
参考答案:D
本题解析:水是弱电解质,存在电离平衡。加热促进电离,所以氢离子的浓度增加,pH减小,但水仍然是中性的。由于水的离子积常数只与温度有关系,所以水的离子积常数增大,因此正确的答案选D。
点评:判断溶液酸碱性的关键是看溶液则氢离子浓度和OH-浓度的相对大小有关系。pH和7的相对大小以及氢离子浓度和1×10-7 mol/L的相对大小都只有在常温下才能成立,在具体的判断中需要注意。
本题难度:一般
5、选择题 ①pH=0的盐酸②0.5mol・L-1盐酸③0.1mol・L-1的NH4Cl溶液④0.1mol・L-1的NaOH溶液⑤0.5mol・L-1的NH4Cl溶液,以上溶液中水电离的c(H+)由大到小的顺序是(?)
A.⑤③④②①
B.①②③⑤④
C.①②③④⑤
D.⑤③④①②
参考答案:A
本题解析:pH=0的盐酸中 ,0.5mol・L-1盐酸中
,0.5mol・L-1盐酸中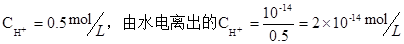 ,0.1mol・L-1的氢氧化钠溶液中
,0.1mol・L-1的氢氧化钠溶液中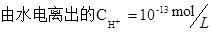 ,NH4Cl溶液中由于铵根离子的水解促进水的电离,,铵根离子的浓度越大促进的能力越强, 所以水电离的c(H+)大小关系为⑤大于③,综上溶液中水电离的c(H+)由大到小的顺序为⑤③④②①,答案选A。
,NH4Cl溶液中由于铵根离子的水解促进水的电离,,铵根离子的浓度越大促进的能力越强, 所以水电离的c(H+)大小关系为⑤大于③,综上溶液中水电离的c(H+)由大到小的顺序为⑤③④②①,答案选A。
本题难度:简单