时间:2017-09-25 19:24:02
1、选择题 常温下,有下列四种溶液:
| ① | ② | ③ | ④ |
| 0.1mol/L NaOH溶液 | pH=11 NaOH溶液 | 0.1mol/L CH3COOH溶液 | pH=3 CH3COOH溶液 |
2、选择题 常温用水稀释0.1mol/l的醋酸钠溶液,溶液中增大的是
[? ]
A.c(H+)
B.c(OH-)·c(H+)
C.c(OH-)
D.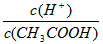
3、选择题 c(N0048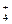 )相同的下列溶液①NH4Cl②(NH4)2SO4?③NH4HSO4?④NH4HCO3,其物质的量浓度由大到小的顺序是()
)相同的下列溶液①NH4Cl②(NH4)2SO4?③NH4HSO4?④NH4HCO3,其物质的量浓度由大到小的顺序是()
A.②④①③
B.②③①④
C.①④③②
D.④①③②
4、选择题 常温下pH=3的二元弱酸H2R溶液与a L pH=11的NaOH溶液混合后,混合液的pH刚好等于7(假设反应前后体积不变),则对反应后混合液的叙述正确的是
A.c(R2-)+ c(OH-)=c(Na+)+c(H+)
B. c(R2-)>c(Na+)>c(H+)=c(OH-)
C.2c(R2-)+ c(HR-)=c(Na+)
D.混合后溶液的体积为2a L
5、选择题 现有浓度均为0.1 mol/L的五种电解质溶液:A.Na2CO3、B.NaHCO3、C.NaAlO2、D.CH3COONa、E.NaOH。
(1)这五种溶液中水的电离程度最大的是?(填编号)。
(2)将五种溶液稀释相同的倍数时,其pH变化最大的是?(填编号)。
(3)将上述A、B、C、D四种溶液两两混合时,有一对溶液相互间能够发生反应,写出该反应的离子方程式:?。
(4)将CO2通入A溶液中恰好呈中性,溶液中2c(CO32-)+c(HCO3-)=?mol/L (设反应前后溶液体积不变)。