时间:2017-09-25 18:52:40
1、选择题 25℃时,将稀CH3COOH逐滴加入到稀NaOH溶液中,当溶液的pH=7时,下列关系不正确的是
A.c(CH3COO-)+ c(CH3COO-)=c(Na+)
B.c(OH-) = c(H+)
C.c(CH3COO-) +c(H+)= c(Na+) +c(OH-)
D.c(Na +)=c(CH3COO-)
2、选择题 已知某温度下CH3COOH的电离常数K=1.6×10-5。该温度下向20 mL 0.01 mol/L CH3COOH溶液中逐滴加入0.01 mol/L KOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关问题: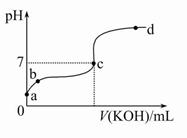
(1)a点溶液中c(H+)为 。
(2)b点溶液中离子浓度大小顺序为 或 或 。c点溶液中的离子浓度大小顺序为 。
(3)a、b、c三点中水的电离程度最大的是 ,滴定过程中宜选用 作指示剂。
3、选择题 下列离子方程式中,属于水解反应的是
[? ]
 HCOO-+ H3O+
HCOO-+ H3O+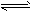 HCO3-+ H+
HCO3-+ H+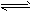 HCO3-+OH-
HCO3-+OH-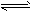 S2-+H3O+
S2-+H3O+ 4、填空题 (12分)(1)氯化铁水解的离子方程式为 ,向氯化铁溶液中加入碳酸氢钠溶液,发现有红褐色沉淀生成,并产生无色气体,其离子方程式为 。
(2)向盛有1mL 0.1mol/L MgCl2溶液的试管中滴加2滴2mol/L NaOH溶液,有白色沉淀生成,再滴加2滴0.1mol/LFeCl3溶液,静置。可以观察到的现象是白色沉淀转变为红褐色沉淀。产生该现象的原因是 。
(3)25℃,向100mL pH=12的NaOH溶液加入pH=10的NaOH溶液1000 mL,混合后溶液体积1100 mL ,pH= 。
(4)常温下,将0.1000 mol L-1 NaOH溶液滴入20.00 mL 0.1000 mol L-1的一元弱酸HA溶液中,刚好完全反应,则c(Na+) c(A-)。(填“>”、“<”或“=”)
(5)某有机物结构为 ,它的含氧官能团名称为 、 。
,它的含氧官能团名称为 、 。
5、选择题 为配置NH4+的浓度与Cl-的浓度比为1:1的溶液,可在NH4Cl溶液中加入( )
① 适量HCl ② 适量NaCl ③ 适量氨水 ④ 适量NaOH
A.①②
B.③
C.③④
D.④