时间:2017-09-25 18:48:46
1、选择题 以下各组表示卤素及其化合物的性质变化规律中,错误的是( )
A.氧化性:F2>Cl2>Br2>I2
B.还原性:Fˉ>Clˉ>Brˉ>Iˉ
C.稳定性:HF>HCl>HBr>HI
D.酸性:HF>HCl>HBr>HI
参考答案:A、同一主族元素,自上而下,元素的非金属性逐渐减弱,其单质的氧化性减弱,故A正确;
B、同一主族元素,自上而下,元素的非金属性逐渐减弱,其阴离子的还原性逐渐增强,故B错;
C、同一主族元素,自上而下,元素的非金属性逐渐减弱,其气态氢化物的稳定性逐渐减弱,故C正确;
D、同一主族元素,自上而下,元素的非金属性逐渐减弱,其气态氢化物的稳定性逐渐减弱,所以HF、HCl、HBr、HI在水中电离的能力依次增强,酸性增强,故D错;
故选:BD.
本题解析:
本题难度:简单
2、选择题 下列价电子表示正确的是
A.29Cu:3d94s2
B.20Ca:3d2
C.39Y :4d15s2
D.26Fe:3d54s2
参考答案:C
本题解析:电子处于全充满或半充满稳定,所以铜的价电子为3d104s1,A不正确。钙原子的最外层电子是4s2,B不正确。铁原子的3d轨道中含有6个电子,D不正确。所以正确的答案是C。
本题难度:困难
3、推断题 a、b、c、d、e是短周期元素,周期表中a与b、b与c相邻;a与e的最外层电子数之比为2:3,b的最外层电子数比e的最外层电子数少1个;常见化合物d2c2与水反应生成c的单质,且溶液使酚酞试液变红。
(1)e的元素符号是__________。
(2)a、b、c的氢化物稳定性顺序为(用分子式表示)__________________;b的氢化物和b的最高价氧化物的水化物反应生成Z,则Z中的化学键类型为__________________,Z的晶体类型为_____________;ab-离子的电子式为____________。
(3)由a、c、d形成化合物的水溶液显碱性,其原因是(用离子方程式表示)_________________________。
(4)一定量的d2c2与ac2反应后的固体物质,恰好与0.8 mol稀盐酸溶液完全反应,并收集到0.25 mol气体,则用物质的量表示该固体物质的组成为__________________、___________________。
参考答案:(1)S
(2)CH4<NH3<H2O;共价键和离子键;离子晶体;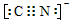
(3)CO32-+H2O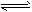 HCO3-+OH-或C2O42-+H2O
HCO3-+OH-或C2O42-+H2O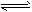 HC2O4-+OH-
HC2O4-+OH-
(4)0.3 mol Na2O2;0.1 mol Na2CO3
本题解析:
本题难度:一般
4、选择题 下列原子序数所对应的元素组中,两者可形成离子键的是
[? ]
A.1和17
B.12和9
C.14和6
D.15和8
参考答案:B
本题解析:
本题难度:简单
5、选择题 “类推”是一种常用的学习方法,但有时会产生错误的结论,下列类推结论中正确的是( )
A.ⅣA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;则ⅤA族元素氢化物沸点顺序也是:AsH3>PH3>NH3
B.第二周期元素氢化物的稳定性序是:HF>H2O>NH3;则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3
C.晶体中有阴离子,必有阳离子;则晶体中有阳离子,必有阴离子
D.干冰(CO2)是分子晶体,则SiO2也是分子晶体
参考答案:A.IVA族元素氢化物不含氢键,分子的相对分子质量越大,沸点越高,则沸点顺序是:GeH4>SiH4>CH4,则VA族元素氢化物中,NH3含有氢键,沸点最高,应为NH3>AsH3>PH3,故A错误;
B.元素的非金属性越强,稳定性越大,同周期元素从左到右元素的非金属性逐渐增强,则对应的氢化物的稳定性逐渐增强,故B正确;
C.金属晶体组成微粒为金属阳离子和自由电子,不含阴离子,故C错误;
D.干冰(CO2)是分子晶体,而SiO2为原子晶体,故D错误.
故选B.
本题解析:
本题难度:简单