时间:2017-09-25 18:38:27
1、选择题 M,N都是短周期元素,原子半径N>M,它们可形成化合物MN2,由此可得出的正确判断是
[? ]
A.M,N可能在同一周期
B.M在N的下一周期
C.M肯定是金属元素
D.N可能在第三周期的ⅥA或ⅦA族
参考答案:C
本题解析:
本题难度:一般
2、选择题 有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+与M2- 具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。下列说法中正确的是
[? ]
参考答案:D
本题解析:
本题难度:一般
3、推断题 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示。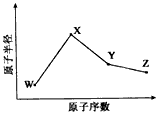
已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大。
(1)X位于元素周期表中第______周期第______族;W的基态原子核外有______个未成对电子。
(2)X的单质子和Y的单质相比,熔点较高的是____________(写化学式);Z的气态氢化物和溴化氢相比,较稳定的是____________(写化学式)。
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是________________________。
(4)在25℃、101 kPa下,已知Y的气态化物在氧气中完全燃烧后恢复至原状态,平均每转移1mol 电子放热190.0kJ,该反应的热化学方程式是________________________。
参考答案:(1)三;IA;2
(2)Si;HCl
(3)SiCl4+3H2O=H2SiO3+3HCl
(4)SiH4(g)+2O2(g)=SiO2(s)+2H2O(l) ΔH=760 kJ/mol
本题解析:
本题难度:一般
4、选择题 能说明A元素的非金属性比B元素的非金属性强的是( )
A.A原子得到电子的数目比B原子少
B.A元素的最高正价比B元素的最高正价要高
C.气态氢化物的稳定性:A比B强
D.A单质能与B的氢化物水溶液反应,生成B单质
参考答案:A.得电子数目多少不能确定非金属性的强弱,故A错误;
B.最高正价不能比较非金属性,如非金属性F>Cl,但F没有正价,故B错误;
C.气态氢化物稳定性可比较非金属性强弱,气态氢化物越稳定非金属性越强,气态氢化物的稳定性:A比B强;所以非金属性:A比B强,故C正确;
D.A单质能与B的氢化物反应生成B单质,则A得电子能力强,非金属性A>B,故D正确;
故选CD.
本题解析:
本题难度:简单
5、选择题 下表是元素周期表的一部分,有关说法不正确的是( )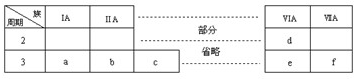
A.元素b的单质不能与酸性氧化物发生化学反应
B.a、b、d、f四种元素的离子半径:f>d>a>b
C.元素c的氧化物既能与酸反应又能与碱反应
D.a、c、e的最高价氧化物对应水化物之间能够相互反应
参考答案:由元素在周期表中的位置可知,a为Na,b为Mg,c为Al,d为O,e为S,f为Cl,
A.因二氧化碳属于酸性氧化物,镁与二氧化碳能反应生成氧化镁和碳,故A错误;
B.电子层越多,离子半径越大,具有相同电子排布的离子,原子序数大的离子半径小,则a、b、d、f四种元素的离子半径:f>d>a>b,故B正确;
C.氧化铝为两性氧化物,则元素c的氧化物为氧化铝,既能与酸反应又能与碱反应,故C正确;
D.a、c、e的最高价氧化物对应水化物分别为NaOH、Al(OH)3、H2SO4,Al(OH)3为两性氢氧化物,则最高价氧化物对应水化物之间能够相互反应,故D正确;
故选A.
本题解析:
本题难度:简单