时间:2017-09-25 18:17:08
1、选择题 在25℃时,用蒸馏水稀释1 mol/L的醋酸溶液至0.01 mol/L,随溶液的稀释,下列说法正确的是
A.溶液中所有离子浓度均减小
B.pH的变化值等于2
C.溶液中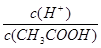 保持增大趋势
保持增大趋势
D.分别与足量的Mg粉反应,0.01 mol/L的醋酸溶液产生的氢气较少
参考答案:C
本题解析:A.醋酸溶液中存在电离平衡,稀释促进电离,氢离子浓度降低。水的离子积常数不变,氢氧根离子浓度增大,A错误;B.由于在稀释过程中氢离子的物质的量增加,则稀释100倍后,pH的变化值小于2,B错误;C.稀释过程中氢离子的物质的量增加,醋酸的物质的量减小,则溶液中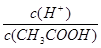 保持增大趋势,C正确;D.稀释过程中醋酸的物质的量不变,则分别与足量的Mg粉反应产生的氢气一样多,D错误,答案选C。
保持增大趋势,C正确;D.稀释过程中醋酸的物质的量不变,则分别与足量的Mg粉反应产生的氢气一样多,D错误,答案选C。
考点:考查醋酸电离平衡的有关判断
本题难度:一般
2、选择题 下列关于电解质溶液的叙述正确的是下列说法正确的是( )
A.CL2和SO2的漂白原理不同,混合使用效果更好
B.测定等浓度的CH3COONa和NaCN溶液的PH值分别为8.8和11.1,可以判断反应CH3COOH+NaCN→CH3COONa+HCN不能发生
C.溶液中滴加盐酸酸化的BaCL2溶液出现白色沉淀,则溶液中一定存在
参考答案:D
本题解析:
本题难度:简单
3、选择题 相同体积的pH=3的强酸溶液和弱酸溶液分别跟足量的镁完全反应
A.强酸溶液产生较多的氢气
B.两者产生等量的氢气
C.无法比较两者产生氢气的量
D.弱酸溶液产生较多的氢气
参考答案:D
本题解析:强酸完全电离,弱酸部分电离。当二者的体积相同,溶液的pH也相同时,弱酸溶液最终电离产生的H+的物质的量多,所以最终与足量的活泼金属Mg发生反应放出的氢气多。因此选项为D。
本题难度:一般
4、选择题 有四种物质:①NaHCO3、②Al(OH)3、③(NH4)2CO3、④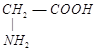 ,其中既能跟盐酸,又能跟NaOH溶液反应的有?
,其中既能跟盐酸,又能跟NaOH溶液反应的有?
A.只有②④
B.只有①②
C.只有①②③
D.①②③④
参考答案:D
本题解析:一般弱酸的酸式盐、弱酸的铵盐、两性混合物、金属铝、氨基酸等既能和盐酸反应,也能和氢氧化钠溶液反应,答案选D。
本题难度:简单
5、填空题 某一元弱酸(用HA表示)在水中的电离方程式是:HA H++A-,回答下列问题:
H++A-,回答下列问题:
(1)向溶液中加入适量NaA固体,以上平衡将向________(填“正”、“逆”)反应方向移动,理由是______________________________________________________。
(2)若向溶液中加入适量NaCl溶液,以上平衡将向________(填“正”、“逆”、“不移动”)反应方向移动,溶液中c(A-)将________(填“增大”、“减小”或“不变”,下同),溶液中c(OH-)将________。
参考答案:(1)逆 c(A-)增大,平衡向减小c(A-)的方向即逆反应方向移动 (2)正 减小 增大
本题解析:(1)HA在水中的电离方程式为HA H++A-,所以向溶液中加入适量NaA固体,溶液中的A-浓度增大,平衡将向逆反应方向移动;
H++A-,所以向溶液中加入适量NaA固体,溶液中的A-浓度增大,平衡将向逆反应方向移动;
(2)若向溶液中加入适量NaCl溶液,以上平衡将向正反应方向移动,因溶液中c(A-)将减小,而溶液中c(OH-)将增大;
本题难度:一般