时间:2017-09-25 18:15:01
1、计算题 (4分)由碳棒,铁片和200mL 1.5mol/L的稀硫酸组成的原电池中,当在碳棒上产生气体3.36L(标准状况)时,则:
①总电池反应的离子方程式为?。
②有?mol电子通过了电线?
③此时溶液中H+的物质的量浓度为?(不考虑溶液体积变化)。
参考答案:①Fe+2H+ = Fe2+ + H2↑②0.3?③1.5mol/L
本题解析:略
本题难度:简单
2、填空题 (12分)某化学兴趣小组对电化学问题进行了实验探究。
I 利用下图装置探究金属的防护措施,实验现象是锌电极不断溶解,铁电极表面有气泡产生。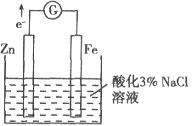
(1)写出负极的电极反应:_____________。
(2)某学生认为,铁电极可能参与反应,并对产物作出假设:
假设1:铁参与反应,被氧化生成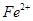 ;
;
假设2:铁参与反应,被氧化生成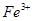 ;
;
假设3:__________________________。
(3)为了探究假设1、2,他进行如下操作:
①取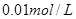
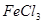 溶液
溶液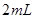 于试管中,加入过量铁粉;
于试管中,加入过量铁粉;
②取操作①试管的上层清液加入2滴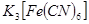 溶液,生成蓝色沉淀;
溶液,生成蓝色沉淀;
③取少量正极附近溶液加入2滴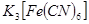 溶液,未见蓝色沉淀生成;
溶液,未见蓝色沉淀生成;
④取少量正极附近溶液加入2滴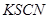 溶液,未见溶液变红。
溶液,未见溶液变红。
据②、③、④现象得出的结论是_____________。
II 利用下图装置做电解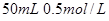 的
的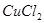 溶液实验。
溶液实验。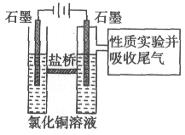
实验记录:
A.阳极上有黄绿色气体产生,该气体使湿润的碘化钾淀粉试纸先变蓝后褪色(提示: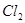 氧化性大于
氧化性大于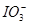 且含
且含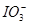 的溶液是无色的);
的溶液是无色的);
B.电解一段时间后,阴极表面除有铜吸附外,还出现了少量气泡和浅蓝色固体。
(1)分析实验记录A中试纸颜色变化,用离子方程式解释:①____________;②_____________。
(2)分析实验记录B中浅蓝色固体可能是_______________(写化学式),试分析生成该物质的原因___________。
参考答案:(共12分)
I (1)Zn―2e一=Zn2+(1分)
(2)铁参与反应,被氧化生成Fe2+和Fe3+(1分)
(3)正极附近溶液不含Fe2+和Fe3+(2分)
II (1)①2I-+Cl2=2Cl-+I2(2分)
②5Cl2+ I2+6H2O=10Cl-+2IO3-+12H+(2分)
(2)Cu(OH)2(2分)电解较长时间后,Cu2+浓度下降,H+开始放电,溶液pH增大,Cu2+转化为Cu(OH)2(2分)
本题解析:I.(1)该装置是原电池,Fe作正极,产生氢气,Zn作负极,失去电子生成锌离子,电极反应式为Zn―2e一=Zn2+;
(2)结合Fe被氧化产物的可能性,所以第三种假设为铁参与反应,被氧化生成Fe2+和Fe3+;
(3)根据反应的现象,与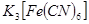 反应产生蓝色沉淀的是亚铁离子,据③考证正极附近溶液中一定不存在亚铁离子;铁离子与KSCN溶液反应,溶液变红色,而④正极附近的溶液,未变红色,所以正极无铁离子,所以据②、③、④现象得出的结论是正极附近溶液不含Fe2+和Fe3+;
反应产生蓝色沉淀的是亚铁离子,据③考证正极附近溶液中一定不存在亚铁离子;铁离子与KSCN溶液反应,溶液变红色,而④正极附近的溶液,未变红色,所以正极无铁离子,所以据②、③、④现象得出的结论是正极附近溶液不含Fe2+和Fe3+;
II.(1)A中的试纸先变蓝色,说明有碘单质生成,后褪色,说明碘单质消失,所以开始的反应是阳极产生的黄绿色气体氯气先氧化碘离子为碘单质,2I-+Cl2=2Cl-+I2,因为氯气的氧化性大于碘酸根离子的氧化性,所以氯气继续氧化碘单质为碘酸根离子,所以蓝色褪去,离子方程式是5Cl2+ I2+6H2O=10Cl-+2IO3-+12H+;
(2)电解氯化铜溶液,阴极先是铜离子放电生成Cu单质,有红色固体析出,随反应的进行,铜离子的浓度减小,氢离子开始放电,使氢氧根离子浓度增大,从而与铜离子反应生成氢氧化铜沉淀,所以B中浅蓝色固体可能是Cu(OH)2。
考点:考查原电池反应原理的应用,反应现象的分析,离子的检验
本题难度:困难
3、选择题 将铁棒和锌棒用导线连接插入硫酸铜溶液中,当电池中有0.4 mol电子通过时,负极的质量变化是
A.增加6.5g
B.减少5.6g
C.增加11.2g
D.减少13g
参考答案:D
本题解析:
专题:电化学专题.
分析:铁棒、锌棒和硫酸铜溶液形成的原电池中,较活泼的金属锌棒作负极,铁棒作正极,负极上锌失电子变成锌离子进入溶液,所以负极质量会减少,正极上铜离子得电子生成铜单质,所以正极上铁棒质量会增加,根据金属和转移电子的关系计算即可.
解答:铁棒、锌棒和硫酸铜溶液形成的原电池中,较活泼的金属锌棒作负极,铁棒作正极,负极上锌失电子质量减少,正极上铜离子得电子质量增加。
设负极上质量减少x,
负极上的电极反应式为:
Zn-2e-=Zn2+
65g 2mol
x? 0.4mol
x=6.5g*0.4mol/2mol=13g,
所以负极质量减少13g,故选D。
点评:本题以原电池原理为载体考查了物质的量的有关计算,难度不大,明确正负极上发生的反应是解本题的关键,然后根据金属质量和转移电子之间的关系计算即可.
本题难度:一般
4、选择题 如下图所示,下列叙述正确的是
A.片刻后CuSO4溶液中的c(SO42―)增大
B.X为正极,发生氧化反应
C.Y与滤纸接触处变红
D.电流沿Cu X
X Y
Y Zn路径流动
Zn路径流动
参考答案:C
本题解析:该原电池的反应本质为Zn+CuSO4=ZnSO4+Cu,活泼金属锌为负极,铜为正极,阴离子向负极移动,故硫酸锌溶液中硫酸根离子浓度增大,A错误;铜为正极,X与正极相连,为电解池的阳极,B错误;Y为阴极,电极反应为2H++2e-=H2,消耗氢离子,溶液显碱性,使酚酞变红,C正确;在溶液中是阳离子的移动方向与电流的方向相同,电子不能在溶液中传导,故D错误,答案选C.
考点:原电池、电解池原理
本题难度:一般
5、填空题 多晶硅是太阳能光伏产业的重要原材料。
(1)由石英砂可制取粗硅,其相关反应的热化学方程式如下:
SiO2(s)+C(s)=SiO(g)+CO(g) ΔH=a kJ・mol-1
2SiO(g)=Si(s)+SiO2(s) ΔH=b kJ・mol-1
①反应SiO2(s)+2C(s)=Si(s)+2CO(g)的ΔH=________ kJ・mol-1(用含a、b的代数式表示)。
②SiO是反应过程中的中间产物。隔绝空气时,SiO与NaOH溶液反应(产物之一是硅酸钠)的化学方程式为________________________________。
(2)粗硅提纯常见方法之一是先将粗硅与HCl制得SiHCl3,经提纯后再用H2还原:
SiHCl3(g)+H2(g)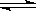 Si(s)+3HCl(g)。
Si(s)+3HCl(g)。
不同温度及不同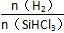 时,反应物X的平衡转化率关系如图所示。
时,反应物X的平衡转化率关系如图所示。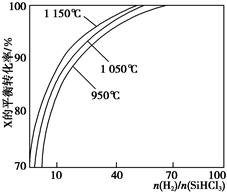
①X是________(填“H2”或“SiHCl3”)。
②上述反应的平衡常数K(1 150 ℃)________K(950 ℃)(填“>”、“<”或“=”)。
(3)SiH4(硅烷)法生产高纯多晶硅是非常优异的方法。
①用粗硅作原料,熔融盐电解法制取硅烷原理如图所示,电解时阳极的电极反应式为_________________________________________。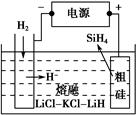
②硅基太阳电池需用N、Si两种元素组成的化合物Y作钝化材料,它可由SiH4与NH3混合气体进行气相沉积得到,已知Y中Si的质量分数为60%,Y的化学式为________。
参考答案:(1)①2a+b ②SiO+2NaOH=Na2SiO3+H2↑
(2)①SiHCl3 ②>
(3)①Si+4H+-4e-=SiH4↑ ②Si3N4
本题解析:(1)①反应SiO2(s)+2C(s)=Si(s)+2CO(g)可由第一个反应×2+第二个反应得到,则ΔH=(2a+b)kJ・mol-1。②根据产物有硅酸钠及质量守恒得到反应的化学方程式为SiO+2NaOH=Na2SiO3+H2↑。(2)①根据图像,在温度不变的情况下,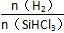 增大,X的平衡转化率增大,则X是SiHCl3。②当
增大,X的平衡转化率增大,则X是SiHCl3。②当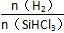 一定时,升高温度,SiHCl3的平衡转化率增大,则表明化学平衡常数K(1 150 ℃)>K(950 ℃)。(3)①电解时阳极发生氧化反应,粗硅失去电子,结合H-生成SiH4气体,则电极反应式为Si+4H--4e-=SiH4↑。②Si、N元素组成的化合物中Si的质量分数为60%,则
一定时,升高温度,SiHCl3的平衡转化率增大,则表明化学平衡常数K(1 150 ℃)>K(950 ℃)。(3)①电解时阳极发生氧化反应,粗硅失去电子,结合H-生成SiH4气体,则电极反应式为Si+4H--4e-=SiH4↑。②Si、N元素组成的化合物中Si的质量分数为60%,则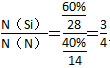 ,即化学式为Si3N4。
,即化学式为Si3N4。
本题难度:一般