时间:2017-09-25 17:53:28
1、选择题 往含等物质的量CO32-和HCO3-的溶液中滴入HCl溶液,下列表示产生的气体在标准状况下的体积与加入的HCl溶液体积关系图正确的是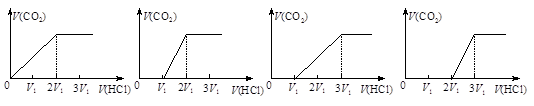 ? A.?B.?C.? D.
? A.?B.?C.? D.
2、填空题 (3分)浓度均为0.1 mol/L的溶液:①HNO3;②H2SO4;③CH3COOH;④Ba(OH)2;?⑤NaOH;⑥CH3COONa;⑦KCl;⑧NH4Cl;⑨NH3・H2O;⑩NaHCO3;溶液的pH由小到大的顺序是:?。(填编号)
3、选择题 化学家借助太阳能产生的电能和热能,用空气和水作原料成功地合成了氨气。下列有关说法正确的是
A.该合成中所有的电能和热能全部转化为化学能
B.该合成氨过程不属于氮的固定
C.空气、水、太阳能均为可再生资源
D.断裂N2中的N≡N键会释放出能量
4、选择题 一些烷烃的燃烧热如下表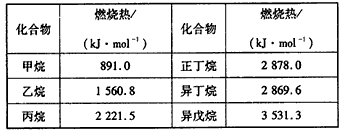
下列表达正确的是
[? ]
A.正戊烷的燃烧热小于3531.3 kJ/mol
B.稳定性:正丁烷>异丁烷
C.乙烷燃烧的热化学方程式为:2C2H6(g) +7O2(g)= 4CO2(g)+6H2O(g);△H=-1560.8 kJ/mol
D.相同物质的量的烷烃CnH2n+2,n越大,燃烧放出的热量越多
5、选择题 常温下,柠檬水溶液的PH是3,其中水电离的c(H+)为
A.1×10-3mol/L
B.1×10-7mol/L
C.1×10-11mol/L
D.1×10-14mol/L