时间:2017-09-25 17:30:32
1、选择题 下列各组物质中,化学键类型不同的是( )
A.CCl4和SO2
B.H2O和NH3
C.CaF2和CsCl
D.NaCl和HNO3
参考答案:A、四氯化碳中碳原子和氯原子之间以共价键相结合,二氧化硫中硫原子和氧原子之间以共价键相结合,所以化学键类型相同,故A不选.
B、水分子中氧原子和氢原子之间以共价键相结合,氨气分子中氮原子和氢原子之间以共价键相结合,所以化学键类型相同,故B不选.
C、氟化钙中钙离子和氟离子之间以离子键相结合,氯化铯中铯离子和氯离子之间以离子键相结合,所以化学键类型相同,故C不选.
D、氯化钠中钠离子和氯离子之间以离子键相结合,硝酸中只含共价键,所以化学键类型不同,故D选.
故选D.
本题解析:
本题难度:一般
2、选择题 下列关于化学键的说法中,正确的是( )
A.只含有共价键的物质一定是共价化合物
B.单质分子中不一定含有化学键
C.NaCl溶于水破坏了离子键,乙醇溶于水破坏了共价键
D.CaCl2?中既有共价键又有离子键
参考答案:A.离子化合物中可以含共价键,如NaOH,故A错误;
B.单原子质分子中不存在化学键,如稀有气体,多原子分子中含有共价键,故B正确;
C.NaCl溶于水破坏了离子键,乙醇溶于水未破坏了共价键,故C错误;
D.氯化镁中只有镁离子和氯离子之间的离子键,故D错误;
故选B.
本题解析:
本题难度:一般
3、选择题 下列化合物中所有化学键都是共价键的是( )
A.Na2O2
B.NaOH
C.H2S04
D.BaCl2
参考答案:A、过氧化钠中钠离子和过氧根离子间存在离子键,氧原子和氧原子之间存在共价键,故A不选;
B、氢氧化钠中钠离子和氢氧根离子之间存在离子键,氧原子和氢原子之间存在共价键,故B不选;
C、硫酸分子中硫原子和氧原子之间存在共价键,氧原子和氢原子之间存在共价键,故C选;
D、氯化钡中氯原子和钡原子之间存在离子键,故D不选;
故选C.
本题解析:
本题难度:简单
4、选择题 2H2(g)+O2(g)===2H2O(l)ΔH=-571.6 kJ・mol-1
CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890 kJ・mol-1
现有H2与CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2和H2O(l)若实验测得反应放出的热量为3695 kJ。则原混合气体中H2与CH4的物质的量之比是
A.1∶1
B.1∶3
C.1∶4
D.2∶3
参考答案:B
本题解析:
试题解析:H2与CH4的混合气体112L,n=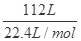 =5mol,设H2与CH4的物质的量分别为x、y,
=5mol,设H2与CH4的物质的量分别为x、y,
2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ?mol-1,
2 571.6kJ
x 285.8x
CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890kJ?mol-1,
1 890kJ
y 890ykJ
则 ,解得x=1.25mol,y=3.75mol,原混合气体中H2与CH4的物质的量之比是1.25mol:3.75mol=1:3,故选B.
,解得x=1.25mol,y=3.75mol,原混合气体中H2与CH4的物质的量之比是1.25mol:3.75mol=1:3,故选B.
考点:有关反应热的计算
本题难度:一般
5、选择题 6.某化学反应的能量变化如下图所示。下列有关叙述正确的是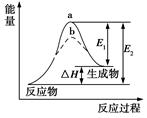
A.该反应为放热反应
B.E2可表示形成新的化学键所释放的能量
C.该反应的反应热ΔH=E1-E2
D.加入催化剂可同等程度的降低E1、E2
参考答案:D
本题解析:反应物的总能量小于生成物的总能量,该反应为吸热反应;E1表示形成新的化学键所释放的能量,E2指反应物化学键断裂所吸收的能量;该反应的反应热ΔH=E2-E1;加入催化剂可降低反应的活化能,即降低E1、E2。
考点:化学反应与能量
点评:本题要弄清楚什么是吸热反应,什么是放热反应,了解反应热的计算方法以及催化剂的作用。
本题难度:一般