ʱ��:2017-09-25 17:12:50
1��ѡ���� ̼�������(CH3OCOOC2H5)��һ�������﮵���л����Һ������̼���������ԭ��Ϊ��C2H5OCOOC2H5(g)+ CH3OCOOCH3(g)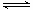 2 CH3OCOOC2H5(g)������������ͬ��CH3OCOOCH3��ƽ��ת����(��)���¶�(T)����Ӧ����ȣ�R=n(C2H5OCOOC2H5):n(CH3OCOOCH3)���Ĺ�ϵ����ͼ��ʾ�����ַ�Ӧ����ȷֱ�Ϊ1:1��2:1��3:1������˵������ȷ����(? )
2 CH3OCOOC2H5(g)������������ͬ��CH3OCOOCH3��ƽ��ת����(��)���¶�(T)����Ӧ����ȣ�R=n(C2H5OCOOC2H5):n(CH3OCOOCH3)���Ĺ�ϵ����ͼ��ʾ�����ַ�Ӧ����ȷֱ�Ϊ1:1��2:1��3:1������˵������ȷ����(? )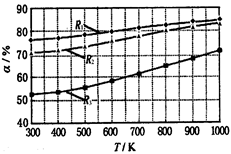
A���÷�Ӧ��H > 0
B��R1��Ӧ�ķ�Ӧ�����Ϊ3:1
C��650�棬��Ӧ�����Ϊ1:1ʱ��ƽ�ⳣ��K = 6
D���÷�ӦΪȡ����Ӧ
�ο��𰸣�C
���������A���������������������£������¶ȣ�CH3OCOOCH3��ƽ��ת��������˵��ƽ�������ƶ�������ƽ���ƶ�ԭ���������¶ȣ���ѧƽ�������ȷ����ƶ�����������Ӧ���������ȷ�Ӧ���÷�Ӧ��H > 0����ȷ��B���������������������£����ӷ�Ӧ���Ũ�ȣ��������������Ӧ���ת���ʣ�����������ת���ʷ������������Ի�������Ӧ����C2H5OCOOC2H5��Ũ�ȣ�������������CH3OCOOCH3��ƽ��ת���ʡ�����R1��ת������ߣ�����R1��Ӧ�ķ�Ӧ�����Ϊ3:1����ȷ��C��650�棬��Ӧ�����Ϊ1:1ʱ��CH3OCOOCH3��ƽ��ת���ʦ�Ϊ60�������������ݻ�ΪVL,��ʼʱ�����ʵ�Ũ��Ϊ��C(C2H5OCOOC2H5)="1/V;" C(CH3OCOOCH3)="1/V;" C(CH3OCOOC2H5)=0����ƽ��ʱC(C2H5OCOOC2H5)=0��4/V; C(CH3OCOOCH3)=0��4/V; C(CH3OCOOC2H5)=1.2/V��K��(1.2/V)2/��0.4/V��2=9������D���ɷ�Ӧ����ʽ�ɿ����÷�ӦΪȡ����Ӧ����ȷ��
�����Ѷȣ�һ��
2��ѡ���� ���ж��ڷ�ӦC��s����H2O��g�� CO��g��+H2��g����������ȷ����
CO��g��+H2��g����������ȷ����
A���ﵽƽ��ʱ������Ӧ���������Ũ����ͬ
B������ѹǿ���Դ˷�Ӧ������Ӱ��
C���ﵽƽ��ʱ��c��H2O����c��CO��=1��1
D���ﵽƽ��ʱ��H2Oת����CO�����ʵ���COת����H2O������
�ο��𰸣�D
�����������
�����Ѷȣ�һ��
3��ѡ���� �ܹ�˵��H2(g)��I2(g) 2HI(g)(HIΪ��ɫ����)�Ѵ�ƽ��״̬����(? )
2HI(g)(HIΪ��ɫ����)�Ѵ�ƽ��״̬����(? )
A��һ��H��H�����ѵ�ͬʱ������H��I���γ�
B��v (H2)���� v (HI) ��ʱ��״̬
C�����º���ʱ����Ӧ��������������ֲ����״̬
D�����º���ʱ����ϵ����ɫ���ٷ����仯��״̬
�ο��𰸣�D
���������A �����ڷ�Ӧ���κ�һ��ʱ����һ��H��H�����ѵ�ͬʱ������H��I���γɣ�B����v (H2)���� v (HI) ��ʱ��״̬Ϊ��Ӧ��һ�������ʱ������ƽ��״̬��C�����º���ʱ�����ڷ�Ӧ���κ�һ��ʱ���Ƿ�Ӧ��������������ֲ����״̬��D��ȷ��
���������⿼���˻�ѧƽ�⣬�Ǹ߿�������ȵ㣬����Ƚϼ�
�����Ѷȣ�һ��
4��ѡ���� һ��������������ܱ������з������·�ӦmA(g)+nB(g) pC(g)����ƽ������¶Ȳ��䣬���������ݻ���С��ԭ����1/2���ﵽ�µ�ƽ��ʱ��C��Ũ��Ϊԭ����1.9��������˵����ȷ����? (? )
pC(g)����ƽ������¶Ȳ��䣬���������ݻ���С��ԭ����1/2���ﵽ�µ�ƽ��ʱ��C��Ũ��Ϊԭ����1.9��������˵����ȷ����? (? )
A��m+n>p
B��A��ת���ʱ��
C��ƽ�������ƶ�
D��C�İٷֺ�������
�ο��𰸣�C
�����������
�����Ѷȣ���
5��ѡ���� ��ij�ܱ������г���1 mol CO ��2 mol H2O(g)��������Ӧ��CO��H2O(g) CO2��H2.����Ӧ�ﵽƽ��ʱ��CO���������Ϊx����ά��������������¶Ȳ��䣬��ʼ���ʰ�����������ȳ���������У��ﵽƽ��ʱCO�������������x����
CO2��H2.����Ӧ�ﵽƽ��ʱ��CO���������Ϊx����ά��������������¶Ȳ��䣬��ʼ���ʰ�����������ȳ���������У��ﵽƽ��ʱCO�������������x����
A��0.5 mol CO��2 mol H2O(g)��1 mol CO2��1 mol H2
B��1 mol CO��1 mol H2O(g)��1 mol CO2��1 mol H2
C��0.5 mol CO��1.5 mol H2O(g)��0.4 mol CO2��0.4 mol H2
D��0.5 mol CO��1.5 mol H2O(g)��0.5 mol CO2��0.5 mol H2
�ο��𰸣�B
������������ڷ�Ӧǰ��������䣬����ֻҪ���Ͷ���CO��ˮ���������ʵ���֮������1�U2��ƽ�⼴ʹ��Ч�ģ���˸��ݷ���ʽ�����ѡ��ABCD�ֱ���1�U2��1�U1��9�U19��1�U2������A��D��ƽ��ʱCO�������������x��B���൱�ڽ���ˮ����Ũ�ȣ�ƽ�����淴Ӧ�����ƶ���ƽ��ʱCO�������������x��C���൱������ˮ����Ũ�ȣ�ƽ��������Ӧ�����ƶ���ƽ��ʱCO���������С��x����ѡB��
�����Ѷȣ�һ��