时间:2017-09-25 17:04:40
1、填空题 (13分)材料1:铁及其化合物在工农业、生活中有广泛的应用。高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂。
(1)已知:4FeO42-+10H2O 4Fe(OH)3+8OH-+3O2。
4Fe(OH)3+8OH-+3O2。
K2FeO4在处理水的过程中所起的作用有?。
(2)将适量K2FeO4溶解于pH=4.74的溶液中,配制成c(FeO42-) =1.0 mmol・L-1的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(FeO42-)的变化,结果见图Ⅰ。该实验的目的是?;发生反应的△H?0(填“>”、“<”或“=”)。
(3)FeO42-在水溶液中的存在形态如图Ⅱ所示。下列说法正确的是?(填字母)。
A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.向pH=10的这种溶液中加硫酸至pH=2,HFeO4-的分布分数逐渐增大
C.向pH=6的这种溶液中加KOH溶液,发生反应的离子方程式为:
HFeO4-+OH-=FeO42-+H2O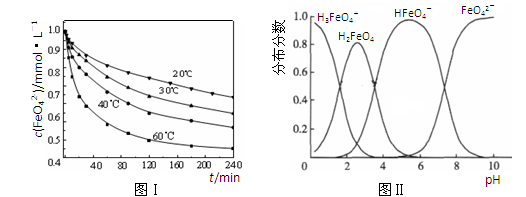
材料2:化合物KxFe(C2O4) y・zH2O(Fe为+3价)是一种光敏感材料,实验室可以用如下方法制备这种材料并测定其组成。
I.制备:
(4)结晶时应将饱和溶液在黑暗处等待晶体的析出,这样操作的原因是?。
(5)操作Ⅲ的名称是?。
Ⅱ.组成测定:
称取0.491g实验所得晶体(假设是纯净物)置于锥形瓶中,加足量蒸馏水和稀H2SO4。将C2O42-完全转化为H2C2O4,用0.10mol・L-1KMnO4溶液进行滴定,消耗KMnO4溶液12.00mL时恰好反应;再加入适量的还原剂,将Fe3+完全转化为Fe2+,用KMnO4溶液继续滴定,当Fe2+完全氧化时,用去KMnO4溶液2.00mL。相关反应如下:
2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O
MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
(6)配制250mL 0.10mol・L-1KMnO4溶液及上述滴定实验中所需的玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒、锥形瓶外还有?和?。两个滴定中到达终点时溶液颜色为?色,且30秒内不变色。
(7)通过计算,求此光敏材料的化学式?。
参考答案:(共13分)
(1)杀菌消毒、吸附悬浮物(或其他合理答案)(各1分,共2分)
(2)探究温度对FeO42-浓度的影响(或其他合理答案)(1分)?>(1分)
(3)C(1分)
(4)黑暗可以防止晶体分解(1分)(5)过滤、洗涤(各1分,共2分)
(6)250mL容量瓶、酸式滴定管(2分)?紫红(1分) (7) K3Fe(C2O4)3・3H2O(2分)
本题解析:(1)K2FeO4中的铁元素化合物高,有很强的氧化性具有杀菌的作用,又因水解可生成胶体,可吸附悬浮物,可用来净水。
(2)(3)均是通过图像收集信息,结合题意及知识的积累进行概念总结。起点高落点低。
(4)(5)(6)考查一些基本的实验操作
(7)MnO4-?+?5Fe2+?+? 8H+?=? Mn2++5Fe3++4H2O
0.0002mol? 0.001mol
2KMnO4?+? 5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O
0.0012mol ?0.003mol
故:可知化学式KxFe(C2O4) y・zH2O的y =3,由化合价进一步可知x=3
由0.491g减去KxFe(C2O4) y・的质量,可求出H2O 的质量为0.054g,即0.003mol
本题难度:一般
2、选择题 把某表面被氧化的钢铁样品,加入过量稀H2SO4中,过滤,除去杂质,在滤中滴加KSCN溶液无血红色,继续向滤液中加入适量硝酸后,再加入过量的氨水,有沉淀生成.上述作过程中加入硝酸之前溶液中的溶质和最终生成的沉淀颜色分别为( )
A.Fe2(SO4)3;白色
B.Fe2(SO4)3;红褐色
C.FeSO4;红褐色
D.FeSO4;色→灰绿色→红褐色
参考答案:C
本题解析:
本题难度:一般
3、选择题 在含Al3+、Fe3+、Fe2+、 的稀溶液中,加入足量Na2O2固体,充分作用后,再加入过量稀盐酸,完全反应,离子数目基本不变的是 (? )
的稀溶液中,加入足量Na2O2固体,充分作用后,再加入过量稀盐酸,完全反应,离子数目基本不变的是 (? )
A.Al3+
B.Fe3+
C.Fe2+
D.
参考答案:A
本题解析:在整个过程中,Al3+的有关反应有:
Al3++4OH-==== +2H2O
+2H2O +4H+Al3++2H2O
+4H+Al3++2H2O
本题难度:一般
4、实验题 (14分)某中学化学课外活动小组欲探究铁在氯气中燃烧产物的成份、性质和用途,设计了如下实验步骤:
(1)用下列实验装置制取干燥纯净的氯气
①制备并收集得到干燥纯净的氯气,上述各装置按气流从左到右方向连接顺序为
?(填仪器接口的字母编号)
②该实验还存在不足之处,应如何改进??
(2)某同学将一定量铁粉与Cl2恰好完全反应得到一固体物质a,然后通过实验确定其成分。探究过程如下:
①提出假设:(请把下列假设补充完整)
假设①:该固体物质是FeCl3;假设②:?;假设③:?。
②设计实验方案:
取少量固体物质a于烧杯中,加适量水溶解,然后取两份a溶液分别进行实验,实验现象与结论如下表,请在表格内的横线处填空。
| 实验方法 | 实验现象 | 结论 |
| 在溶液中加 KSCN溶液 | ? | 固体物质中有FeCl3 |
| 向a溶液中滴加 酸性KMnO4溶液 | KMnO4溶液紫色 不褪色 | 固体物质中不含______ |

参考答案:(14分)(1)①aedbcgf (2分)?②在C后接NaOH溶液尾气处理装置(1分)
(2)(1)FeCl2(1分);FeCl3和FeCl2的混合物(1分)
(2)
实验方法
实验现象
结论
在溶液中加
KSCN溶液
溶液为红色(1分)
固体物质中有FeCl3
向a溶液中滴加
酸性KMnO4溶液
KMnO4溶液紫色
不褪色
固体物质中不含FeCl2(1分)
由此得出结论:假设?①?结论成立(1分)
(3)A D(2分)?(4) (2分),1.12L(2分)
(2分),1.12L(2分)
本题解析:(1)①由于浓盐酸易挥发,所以生成的氯气中含有氯化氢,可以通过饱和食盐水除去。干燥氯气可以浓硫酸。由于氯气的密度大于空气的,所以应该用向下排空气发收集,即正确的顺序是aedbcgf 。
②由于氯气是有毒气体,应该有尾气处理装置,即在C后接NaOH溶液尾气处理装置。
(2)①由于铁元素有两种价态+2价和+3价,所以假设2和3分别是FeCl2;FeCl3和FeCl2的混合物。
②在溶液中铁离子能和KSCN溶液发生反应,使溶液显红色;酸性高锰酸钾溶液具有强氧化性,能氧化亚铁离子。由于实验中酸性高锰酸钾溶液不褪色,说明固体中不存在氯化亚铁,因此假设①是正确的。
(3)根据沉淀转化的特点:向溶解度更小的方向转化可知,选项A正确;B不正确,氯化亚铁在溶液中显浅绿色,因此实验现象应该是溶液颜色由黄色变成浅绿色;C不正确,得到的是氢氧化铁胶体;氯化铁水解,加热促进水解,且氯化氢极易挥发,实验最终得到的是氢氧化铁,灼烧得到氧化铁,D正确,答案选AD。
(4)原电池中负极失去电子,所以甲烷在负极通入。由于电解质是氢氧化钾,因此负极反应式是 。电解池中阴极铜离子放电,阳极Cl-放电,电极反应式分别是Cu2++2e-=Cu、2Cl--2e-=Cl2↑。生成铜是3.2g,转移电子是0.1mol,所以生成氯气是0.05mol,标准状况下的体积是0.05mol×22.4L/mol=1.12L。
。电解池中阴极铜离子放电,阳极Cl-放电,电极反应式分别是Cu2++2e-=Cu、2Cl--2e-=Cl2↑。生成铜是3.2g,转移电子是0.1mol,所以生成氯气是0.05mol,标准状况下的体积是0.05mol×22.4L/mol=1.12L。
本题难度:一般
5、选择题 下列物质不能与氢氧化钠溶液反应的是( )
A.Fe2O3
B.Al(OH)3
C.NaHCO3
D.H2SiO3
参考答案:A
本题解析:
本题难度:简单