时间:2017-09-25 16:52:31
1、填空题 已知:
①N2 (g)+3H2 (g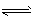 )2NH3 (g) △H = -92. 4 kJ/mol
)2NH3 (g) △H = -92. 4 kJ/mol
②2H2 (g)+SO2 (g)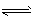 S(g)+2H2O(g) △H=90. 4kJ/mol
S(g)+2H2O(g) △H=90. 4kJ/mol
③2H2 (g)+CO(g)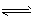 CH3OH(g) △H=-90.8 kJ/mol
CH3OH(g) △H=-90.8 kJ/mol
请回答:
(1)上述变化过程中放出热量的是____(填序号,下同),吸收热量的是___。
(2)4 g H2 (g)完全反应生成甲醇气体时,△H=___kJ/mol。
(3)生成1 mol NH3 (g)的反应热为____kJ/mol。
参考答案:(1)①③;②
(2) -90. 8
(3) -46. 2
本题解析:
本题难度:一般
2、选择题 最近意大利罗马大学的Fulvio?Cacace等人获得了极具理论研究意义的N4分子.N4分子结构如图,已知断裂1molN-N吸收167kJ热量,生成1mol?N≡N放出942kJ热量.根据以上信息和数据,则由N2气体生成1mol气态N4的△H为( ? )
A.-441kJ?mol-1
B.+441kJ?mol-1
C.-882kJ?mol-1
D.+882kJ?mol-1
参考答案:D
本题解析:
本题难度:简单
3、选择题 已知A(g)+B(g)=C(g) ΔH=-Q1 kJ・mol-1,D(g)+B(g)=E(g) ΔH=-Q2 kJ・mol-1,且Q1>Q2,若A和D的混合气体1 mol完全与B反应,放出热量Q3 kJ,则A和B的物质的量之比为
[? ]
A.(Q2-Q1) ∶ (Q1-Q3)
B.(Q3-Q2) ∶ (Q1-Q3)
C.(Q3-Q2) ∶ (Q3-Q1)
D.(Q1-Q2) ∶ (Q3-Q1)
参考答案:B
本题解析:
本题难度:一般
4、选择题 已知1?mol红磷转化为1?mol白磷,吸收18.39?kJ热量. 4P(红,s)+5O2(g)===2P2O5(s) ΔH1 4P(白,s)+5O2(g)===2P2O5(s) ΔH2 则ΔH1与ΔH2的关系正确的是
[? ]
A.ΔH1=ΔH2?
B.ΔH1>ΔH2
C.ΔH1<ΔH2?
D.无法确定
参考答案:B
本题解析:
本题难度:一般
5、简答题 已知120克碳燃烧所得气体中,CO占1/3体积,CO2占2/3体积,且C(s)+1/2O2(g)=CO(g)△H=-110kJ/mol;CO(g)+1/2O2(g)=CO2(g)△H=-283kJ/mol.计算:
(1)该情况下燃烧120克碳所放出的热量是多少?
(2)与这些碳完全燃烧相比较,损失的热量是多少?
参考答案:(1)已知:C(s)+1/2O2(g)=CO(g)△H=-110kJ/mol;
CO(g)+1/2O2(g)=CO2(g)△H=-283kJ/mol;
两式相加可得碳燃烧生成二氧化碳的热化学方程式:C(g)+O2(g)=CO2(g)△H=-393kJ/mol;
120克碳的物质的量为120g12g/mol=10mol,根据C元素守恒可知CO、CO2总的物质的量为10mol,故CO为10mol×13=103mol,
CO2为10mol×23=203mol,故放出的热量为:103mol×110kJ/mol+203mol×393kJ/mol=2986.7kJ/mol,
答:该情况下燃烧120克碳所放出的热量是2986.7kJ;
(2)该燃烧情况与碳完全燃烧相比较,损失的热量等于CO燃烧放出的热量为:103mol×283kJ/mol=943.3kJ;
答:损失的热量为943.3kJ.
本题解析:
本题难度:一般