时间:2017-09-25 16:51:03
1、填空题 元素周期表是学习物质结构和性质的重要工具,下图是元素周期表的一部分,表中所列字母A、D、F、G、Q、M、R、N、T分别代表某种化学元素。请依据这9种元素回答下列问题。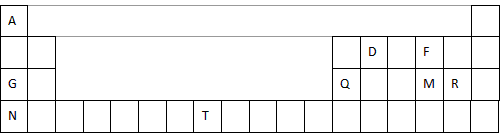
(1)表中T的元素符号为___________ ,金属性最强的元素是_________ (填元素符号)。
(2)元素的非金属性:M_________ R(填“>”或“<”)。
(3)R的最高价氧化物对应水化物的化学式是__________ 。
(4)F、G两元素形成的淡黄色固体物质的电子式为_______,该物质含有的化学键的类型是________。
(5)表中某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是 ___________(填离子符号)。
(6)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为________ 。
(7)A与D形成分子的空间结构可能是(填序号)________ 。 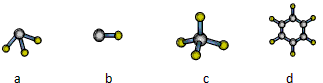
2、推断题 已知X、Y、Z、W四种元素分别是元素周期表中连续三个短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键,试推断:
(1)X、Z两种元素的元素符号:X__________________、Z______________________。
(2)由以上元素中两两形成的化合物中:溶于水显碱性的气态氢化物的电子式为________________,它的共价键属于________(填“极性”或“非极性”)键;含有离子键和非极性共价键的化合物的电子式为________________________________。
(3)由X、Y、Z三元素可以形成一种常见的离子化合物,由X、Z、W三元素可以形成另一种离子化合物,则两种化合物的浓溶液混合共热的离子反应方程式为__________________。
(4)X与W形成的离子化合物溶于水,发生反应的化学方程式为 _______________________,其中水作________剂(填“氧化”或“还原”)。
3、选择题 下列过程中,没有明显实验现象的是( )
A.向Fe(NO3)2溶液中滴加稀硫酸
B.将HCl通入NaAlO2溶液中
C.加热溶有SO2的品红溶液
D.向碳酸氢钠溶液中滴加氢氧化钠溶液
4、选择题 下列各组物质发生化学反应时,由于反应物的量不同而导致生成不同产物的是(?)
①CO2与NaOH溶液
②盐酸溶液与偏铝酸钠
③NaHCO3溶液与盐酸
④C与O2
⑤AlCl3溶液与氢氧化钠溶液
A.除③外
B.除②外
C.除②③⑤外
D.除②⑤外
5、填空题 下列微粒之间,属于同位素的是______,属于同素异形体的是______,属于同分异构体的是______,固体时属于同种晶体的是______.
A.正丁烷与异丁烷、B.红磷与白磷、C.氕与氚、D.氯化钠与干冰、E.金刚石与水晶、F.氧气和臭氧、
G.13C和14C、H.CH3CH(CH3)CH2CH(CH3)CH3和CH3C(CH3)2CH2CH2CH3.