时间:2017-09-25 16:42:23
1、选择题 下列性质中,可以证明某化合物是离子化合物的是( )
A.可溶于水
B.具有较高的熔点
C.其水溶液能导电
D.其固体不导电,熔融状态能导电
2、选择题 下列现象或事实能说明分子之间有间隔的是。
A.用手捏气球,可以使气球变瘪。
B.墙内开花墙外香。
C.100ml的水与100ml的酒精混合,所得溶液的体积小于200ml 。
D.将稀盐酸倒在大理石可以观察到气泡。
3、填空题 下面是C60、金刚石和二氧化碳的分子模型。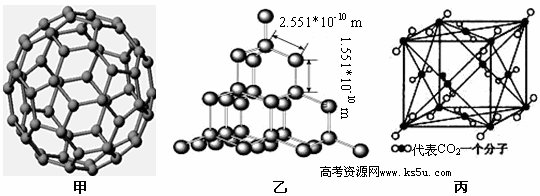
请回答下列问题:
(1)硅与碳同主族,写出硅原子基态时的核外电子排布式:_________________
(2)从晶体类型来看,C60属于_________晶体。
(3)二氧化硅结构跟金刚石结构相似,即二氧化硅的结构相当于在硅晶体结构中每个硅与硅的化学键之间插入一个O原子。观察图乙中金刚石的结构,分析二氧化硅的空间网状结构中,Si、O原子形成的最小环上O原子的数目是__________________________;晶体硅中硅原子与共价键的个数比为?
(4)图丙是二氧化碳的晶胞模型,图中显示出的二氧化碳分子数为14个。实际上一个二氧化碳晶胞中含有________个二氧化碳分子,二氧化碳分子中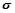 键与
键与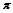 键的个数比为?。
键的个数比为?。
(5)有机化合物中碳原子的成键方式有多种,这也是有机化合物种类繁多的原因之一。丙烷分子中2号碳原子的杂化方式是_______,丙烯分子中2号碳原子的杂化方式是_______,丙烯分子中最多有?个原子共平面。
4、选择题 下列说法中正确的是( )?
A.难失电子的原子,获得电子的能力一定强?
B.易得电子的原子所形成的简单阴离子,其还原性一定强?
C.分子中键能越大,键长越长,则分子越稳定?
D.电子层结构相同的不同离子,核电荷数越多半径越小
5、填空题 数10亿年来,地球上的物质不断地发生变化,大气的成分也发生了很大变化。下表是原始大气和目前空气的主要成分 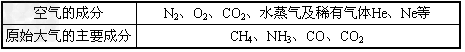
用上表所涉及的分子填写下列空白。
(1)含有10个电子的分子有(填化学式,下同)____;
(2)由极性键构成的非极性分子有____;
(3)与H+可直接形成配位键的分子有____;
(4)沸点最高的物质是____,用所学知识解释其沸点最高的原因____;
(5)分子中不含孤对电子的分子(除稀有气体外)有____,它的立体构型为________;
(6)极易溶于水、其水溶液呈碱性的物质的分子是____,它之所以极易溶于水是因为它的分子和水分子之间可形成____;
(7)CO的结构可表示为OC,与CO结构最相似的分子是____,这两种结构相似的分子中,分子的极性____(填“相同”或“不相同”),CO分子中有一个键的形成与另外两个键不同,它叫________。