时间:2017-09-25 16:20:39
1、填空题 (11分)短周
 期主族元素A、B、C、D、E原子序数依次增大,A元素单质常温常压下是最轻的气体,B元素所形成化合物种类最多,C的最高价氧化物对应水化物甲与其气态氢化物乙能够化合形成盐丙;D元素的离子半径是同周期元素形成的简单离子中最小的。
期主族元素A、B、C、D、E原子序数依次增大,A元素单质常温常压下是最轻的气体,B元素所形成化合物种类最多,C的最高价氧化物对应水化物甲与其气态氢化物乙能够化合形成盐丙;D元素的离子半径是同周期元素形成的简单离子中最小的。
(1)已知相关物质之间存在如下变化: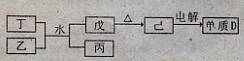
①丁与乙和水反应生成戊和丙的离子方程式为?,由物质已电解得到单质D的化学方程式为?;
②0.lmoL/L的丙溶液中所含离子浓度由大到小排列顺序为?。
(2)已知E及其化合物有以下变化:
写出单质E与化合物Z在一定条件下反应生成.X和水的化学方程式?。
由A、B、C、D、E5种元素中的.两种元素,可形成既含极性键又含非极性键的18电子的分子,该分子的分子式为____?(任写一个即可)。
(3)C有多种氧化物,其中之一是一种无色气体,在空气中迅速变成红棕色,在一定条件下,2L的该无色气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液全吸收后没有气体残留, 所生成R的含氧酸盐只有一种,则该含氧酸盐的化学式是?。
所生成R的含氧酸盐只有一种,则该含氧酸盐的化学式是?。
参考答案:
本题解析:略
本题难度:困难
2、填空题 (16分)已知:A为常见的短周期轻金属,含A的合金材料常用于火箭、飞机、轮船等制造业;B是一种盐,在工农业生产中用途较广;C、F、H为常见非金属单质;常温下C、F、I、E、J和K为气体;E对空气的相对密度为0.586;G为液体。有关物质间的转化关系如下(图中部分反应物或产物已省略):
请填空:
(1)B的电子式为?;I分子的空间构型为?
(2)反应②的实验现象为?
(3)操作a必须在HCl气流中加热得无水物,其原因是?;操作b为?
(4)反应①的离子反应方程式为?;反应③的化学反应方程式为?
(5)已知C的燃烧热为286KJ/mol,请写出表示1g C在F中完全燃烧生成液体G的热化学反应方程式? .。
参考答案:(16分)
(1)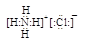 (2分)直线形(2分)
(2分)直线形(2分)
(2)燃烧,发光发热;产生黑色和白色固体物质(见“燃烧”1分,见“黑色”1分)(2分)
(3)抑制Mg2+的水解(2分,写方程式同样给分),熔融状态下电解(2分)
(4)Mg+2NH4+==Mg2++H2↑+2NH3↑?(2分)
4NH3+5O2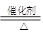 4NO+6H2O?(2分)
4NO+6H2O?(2分)
(5)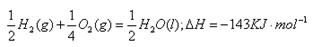 2分)
2分)
本题解析:短周期轻金属,含A的合金材料常用于火箭、飞机、轮船等制造业,可知A为Mg;
本题的突破口之一:E对空气的相对密度为0.568即得E的相对分子质量为17,即为NH3;由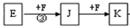 可推断F为O2;则J为NO;K为NO2;又因G为液体,则G为H2O;进而可推得L浓溶液为HNO3溶液;
可推断F为O2;则J为NO;K为NO2;又因G为液体,则G为H2O;进而可推得L浓溶液为HNO3溶液;
本题的突破口之二: 已推知G为H2O、F为O2;则C为H2、H为C;
已推知G为H2O、F为O2;则C为H2、H为C;
本题的突破口之三: 黄绿色气体为CL2,则可得D溶液为MgCL2;而
黄绿色气体为CL2,则可得D溶液为MgCL2;而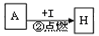 可推知I为CO2气体;
可推知I为CO2气体;
最后可分析得出B为NH4CL,K为KNO3。
本题难度:简单
3、推断题 下图涉及多种无机化工反应,所涉及物质都是由短周期元素组成的,其中R是一种新型无机材料,M是一种应用广泛的金属材料,F是人工合成的第一种有机物,且是一种常见的化肥,A、C、D、M均为常见元素的单质,“↑”表 示该物质常温下是气体,反应G+J→F+H2O中G与J的最佳配比为2:1,向Y溶液中通入足量的J气体时可得到一种白色胶状沉淀,将该白色胶状沉淀滤出,洗净后加热分解可以得到B。 
请回答下列问题:
(1)写出B的化学式:____ ,F的化学式:____ 。
(2)反应①的化学方程式为___。
(3)反应④的离子方程式为____ 。
(4)上述反应中属于非氧化还原反应的___(填写相应反应的序号)。
(5)Y溶液呈___性(填“酸”、“碱”或“中”),用离子方程式解释:____。
参考答案:(1) Al2O3?; CO( NH2)2
(2)N2 +Al2O3 +3C 3CO +2AlN
3CO +2AlN
(3)AlN+OH- +H2O=AlO2-+NH3↑
(4)④⑦
(5)碱; AlO2-+2H2O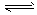 Al(OH) 3 +OH -
Al(OH) 3 +OH -
本题解析:
本题难度:一般
4、推断题 下列①-⑩分别代表有关反应中的一种物质,它们均是中学化学中常见物质。已知①-⑤和⑥-⑩分别含有同一种元素: 
(1)分别写出①、④、⑧、⑩的化学式或离子符号: ①______;④_______;⑧_______;⑩______。
(2)写出下列反应方程式,是离子反应的写出离子方程式:
① + OH- ________________________。
________________________。
① + ⑥  _____________________。
_____________________。
参考答案:(1) ①Al ;④Al(OH)3; ⑧Fe2+ ;⑩Fe(OH)2
(2)2Al+2OH-+2H2O==2AlO2-+3H2↑;2Al+Fe2O3 2Fe+Al2O3
2Fe+Al2O3
本题解析:
本题难度:一般
5、简答题 金属及其化合物的种类很多,我们可以按照“金属单质、金属氧化物、金属氢氧化物、盐”的类别进行研究.以下是某种金属及其化合物之间的转化关系(“→”所指的转化都是一步完成)
(1)写出以下物质的化学式:A______,C______.
(2)A与水反应的离子方程式:______.
(3)若B为呼吸面具中的供养剂,其供养时主要反应的化学方程式:______.
(4)写出一种“C→D”转化的化学方程式:______.
参考答案:金属单质可以形成氧化物,也可以直接生成氢氧化物碱、金属氧化物可以形成碱、金属氢氧化物一步形成盐,解题关键在金属单质可以直接形成碱的推断.A为活泼金属K、Ca、Na、Mg等;各步反应都需要一步形成;
(1)依据判断A、C物质的化学式为A为Na;C为NaOH;故答案为:Na;NaOH;
(2)A为钠.与水反应的化学方程式为:2Na+2H2O=4NaOH+H2↑;故答案为:2Na+2H2O=2NaOH+H2↑;
(3)若B为呼吸面具中的供养剂,其供养时主要反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2↑;
故答案为:2Na2O2+2CO2=2Na2CO3+O2↑;
(4)C→D转化的化学方程式为:NaOH+HCl=NaCl+H2O;故答案为:NaOH+HCl=NaCl+H2O;
本题解析:
本题难度:一般