时间:2017-09-25 16:18:50
1、填空题 煤化工中常需研究不同温度下的平衡常数、投料比及产率等问题。已知:
CO(g)+H2O(g) ?CO2(g)+H2(g)的平衡常数随温度的变化如下表:
?CO2(g)+H2(g)的平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |

参考答案:(每空2分,共10分)(1)放热(2分)?(2)增大(2分);增大(2分)
(3)B、C(2分,选一个且正确给1分,有错选不给分)?(4)60%(2分)
本题解析:(1)根据表中数据可知,随着温度的升高,平衡常数逐渐减小。这说明升高温度,平衡向逆反应方向移动,因此正反应是放热反应。
(2)保持容器体积不变升高温度,正反应速率增大,但逆反应速率增大的程度更大,所以平衡向逆反应方向移动。由于气体的物质的量是不变的,但温度升高,所以容器内气体的压强增大。
(3)根据表中数据可知,选项C中由于没有生成物,所以反应一定是向正反应方向进行的。而选项A、B、D中此时离子积分别是 。由于830℃是平衡常数是1,所以选项A是向逆反应方向进行的,B是向正反应方向进行的,而D恰好是平衡状态,答案选BC。
。由于830℃是平衡常数是1,所以选项A是向逆反应方向进行的,B是向正反应方向进行的,而D恰好是平衡状态,答案选BC。
(4)设达到平衡时,CO的转化率是x,则消耗CO和水蒸气都是4x,而生成CO2和氢气都是4x,所以根据平衡常数表达式可知 ,解得x=60%。
,解得x=60%。
本题难度:一般
2、选择题 下列叙述中,不能用平衡移动原理解释的是
A.红棕色的NO2,加压后颜色先变深后变浅
B.高压比常压有利于合成SO3的反应
C.加入催化剂有利于氨的合成
D.工业制取金属钾 Na(l)+ KCl(l)  NaCl(l)+ K(g)选取适宜的温度,使K成蒸气从反应混合物中分离出来
NaCl(l)+ K(g)选取适宜的温度,使K成蒸气从反应混合物中分离出来
参考答案:C
本题解析:略
本题难度:一般
3、选择题 将4mol A气体和2mol B气体在2L的密闭容器中混合,并在一定条件下发生如下可逆反应:2A(g) + B(g) 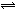 ?2C(g)。若经2s后测得C的浓度为0.6 mol/L,现有下列几种说法,其中正确的是(?)
?2C(g)。若经2s后测得C的浓度为0.6 mol/L,现有下列几种说法,其中正确的是(?)
A.反应达到平衡时,A、B、C的浓度不再变化,反应停止
B.升高温度、增大压强、增加A的浓度、减小C的浓度或使用催化剂等都可以使反应速率加快
C.经过足够长时间后,A和B可以完全转化为C
D.2s时物质A转化了1.2mol
参考答案:D
本题解析:A、反应达到平衡时,A、B、C的浓度不再变化,化学平衡是动态平衡,反应仍在继续,故A错误;
B、减小浓度,反应速率减小,故B错误;
C、反应是可逆反应,反应物不能全部转化为生成物,故C错误。
故选D。
点评:本题考查了化学平衡状态的判断及外界条件对化学平衡的影响,难度不大,注意反应达到平衡状态时,正逆反应速率相等但不等于0。
本题难度:简单
4、选择题 随着汽车数量的逐年增多,汽车尾气污染已成为突出的环境问题之一。反应:2NO(g)+2CO(g) 2CO2(g)+N2(g)可用于净化汽车尾气,已知该反应速率极慢,570 K时平衡常数为1×1059。下列说法正确的是( )
2CO2(g)+N2(g)可用于净化汽车尾气,已知该反应速率极慢,570 K时平衡常数为1×1059。下列说法正确的是( )
A.提高尾气净化效率的最佳途径是研制高效催化剂
B.提高尾气净化效率的常用方法是升高温度
C.装有尾气净化装置的汽车排出的气体中不再含有NO或CO
D.570 K时及时抽走CO2、N2,平衡常数将会增大,尾气净化效率更佳
参考答案:A
本题解析:“该反应速率极慢”,故提高尾气净化效率的最佳途径是研制高效催化剂,A说法正确;升高温度的措施在处理尾气时难以实现,故B错;该反应是可逆反应,故C错;平衡常数只与温度有关,故D错。
本题难度:一般
5、选择题 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是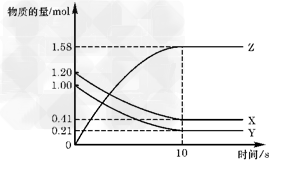
[? ]
A.反应开始到10s,用Z表示的反应速率为0.158mol/(L・s)
B.反应开始时10s,X的物质的量浓度减少了0.79mol/L
C.反应开始时10s,Y的转化率为0.79(转化率=参加反应的物质的物质的量÷该物质的起始物质的量)
D.反应的化学方程式为:X(g)+Y(g) Z(g)
Z(g)
参考答案:C
本题解析:
本题难度:一般