时间:2017-09-24 01:19:47
1、选择题 某溶液中只含有Na+、H+、OH-、A-四种离子,下列说法正确的是
[? ]
A、若溶液中c(A-)= c(Na+),则溶液一定呈中性
B、溶液中不可能存在:c(Na+)> c(A-)> c(OH-)> c(H+)
C、若c(OH-)> c(H+),溶液中不可能存在:c(Na+) > c(OH-) > c(A-) > c(H+)
D、若溶质为NaA、HA,则一定存在:c(A-)> c(Na+)> c(H+)> c(OH-)
参考答案:A
本题解析:
本题难度:一般
2、填空题 1mol?Na2SO4中含有______molNa+,含有______个SO42-,其中Na2SO4的质量为______g.Al2(SO4)3?的电离方程式为______,在______?mol?Al2(SO4)3中含0.3molSO42-,其中含Al3+______mol.
参考答案:解;硫酸钠的电离方程式为:
Na2SO4 =2Na++SO42-
?1? 2? 1
?1mol?2mol?1mol
N(SO42-)=n NA=1mol×6.02×1023个/mol=6.02×1023个;
m(?Na2SO4)=n×M=1mol×142g/mol=142g;
Al2(SO4)3?是强电解质,完全电离,电离方程式为:Al2(SO4)3=2Al 3++3SO42-
Al2(SO4)3 =2Al3++3SO42-
?1? ? 2? 3
0.1mol? 0.2mol? 0.3mol
故答案为:2;6.02×1023;? 142;?Al2(SO4)3=2Al 3++3SO42-; 0.1;0.2.
本题解析:
本题难度:一般
3、选择题 下列电离方程式书写正确的是
A.H2S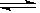 2H++S2-
2H++S2-
B.Al(OH)3==Al3+ + 3OH-
C.NH3・H2O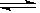 NH4+ +OH-
NH4+ +OH-
D.NaHCO3 ==Na++ H+ + CO32-
参考答案:C
本题解析:A错,二元弱酸应分步电离;B错,应用可逆符号;C正确;D错,碳酸氢根离子不拆;
本题难度:一般
4、简答题 有以下几种物质①NaCl(l)?②HCl(l)?③水银?④蔗糖?⑤液态醋酸⑥KNO3溶液?⑦氯气⑧液态SO3⑨纯水⑩熔融KOH,填空回答(填序号):以上物质中能导电的是______;属于电解质的是______;属于非电解质的是______;属于弱电解质的是______.
参考答案:①NaCl(l)中存在自由移动的离子,能导电,且属于化合物,则属于电解质,熔化时完全电离属于强电解质;
②HCl(l)中不存在带电的微粒,不能导电,但其符合水溶液能导电的化合物,则属于电解质,在水中完全电离,则属于强电解质;
③水银中存在自由移动的电子,能导电,但属于单质,则既不是电解质,也不是非电解质;
④蔗糖中不存在带电微粒,不导电,且是在水溶液中和熔化状态下都不能导电的化合物,则属于非电解质;
⑤液态醋酸中不存在带电的微粒,不能导电,但其符合水溶液能导电的化合物,则属于电解质,又在水中不能完全电离,则属于弱电解质;
⑥KNO3溶液中存在自由移动的离子,能导电,但溶液属于混合物;
⑦氯气是由分子构成的物质,不导电,且属于单质;
⑧液态SO3中不存在带电微粒,不导电,在水中发生电离不是其本身,则属于非电解质;
⑨纯水几乎不导电,能微弱电离,则属于弱电解质;
⑩熔融KOH中存在自由移动的离子,能导电,且属于化合物,则属于电解质,熔化时完全电离属于强电解质;
故答案为:①③⑥⑩;①②⑤⑨⑩;④⑧;⑤⑨.
本题解析:
本题难度:一般
5、选择题 下列溶液中微粒的物质的量浓度关系不正确的是( )
A.将1molCl2全部溶入水形成的1L溶液中:2c(Cl2)+c(Cl-)+c(HClO)+c(ClO-)=2mol/L
B.Na2CO3溶液:c(OH-)-c(H+)=c(HCO3-)+c(H2CO3)
C.物质的量浓度均为0.1mol/L的NaClO与NaHCO3组成的混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-)
D.室温下,向0.01mol/L的NH4HSO4溶液中滴加NaOH溶液至呈中性:c(Na+)>c(SO42--)>c(NH4+)>c(OH-)=c(H+)
参考答案:B
本题解析:
本题难度:简单