时间:2017-09-24 01:19:07
1、选择题 NaCl的晶胞如图,每个NaCl晶胞中含有的Na+离子和Cl-离子的数目分别是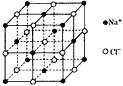
[? ]
A.14,13
B.1,1
C.4,4
D.6,6
参考答案:C
本题解析:
本题难度:一般
2、填空题 晶胞即晶体中最小的重复单元。已知铜为面心立方晶体,其结构如图I所示,面心立方的结构特征如图Ⅱ所示。若铜原子的半径为1.27×10-10m,试求铜金属晶体中的晶胞边长,即图Ⅲ中AB的长度为_______m。 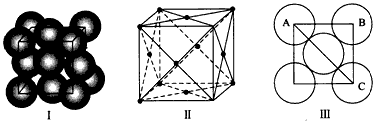
参考答案:3.59×10-10
本题解析:
本题难度:一般
3、选择题 已知X、Y、Z三种元素组成的化合物是离子晶体,其晶胞如图所示,则该化合物的化学式正确的是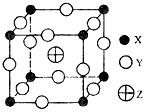
[? ]
A.ZXY3
B.ZX2Y6
C.ZX4Y8
D.ZX8Y12
参考答案:A
本题解析:
本题难度:一般
4、选择题 下列叙述正确的是(?)
A.原子晶体中,共价键的键能越大,熔沸点越高
B.分子晶体中,分子间作用力越大,该分子越稳定
C.分子晶体中,共价键键能越大,熔沸点越高
D.某晶体溶于水中,可电离出自由移动的离子,该晶体一定是离子晶体
参考答案:A
本题解析:A、原子晶体中,原子间以极强的共价键结合。共价键越强,结合的越牢固,共价键的键能越大,断裂共价键消耗的能量就越高,熔沸点越高。正确。B、分子晶体中,分子间以分子间作用力结合。分子间作用力越大,破坏分子间作用力使物质融化或汽化消耗的能量就越高。即该晶体的熔沸点越高。错误。C、分子晶体中,共价键键能越大,分子就越稳定。错误。D、某晶体溶于水中,可电离出自由移动的离子,该晶体可能是离子晶体,也可能是分子晶体。错误。
本题难度:一般
5、选择题 钡在氧气中燃烧时得到一种钡的氧化物晶体,其结构如下图所示,有关说法正确的是(?)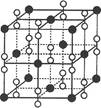
A.该晶体为分子晶体
B.晶体的化学式为Ba2O2
C.该氧化物的电子式为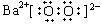
D.与每个Ba2+ 距离相等且最近的Ba2+ 共有6个
参考答案:C
本题解析:钡是活泼的金属,形成的氧化物是离子晶体,选项A不正确;根据晶胞可知钡原子的个数是12×1/8+6×1/2=4,而O22-的形成存在的,共计是4个,是以化学式应该是BaO2 ,选项B不正确,而选项C正确;与每个Ba2+ 距离相等且最近的Ba2+ 共有12个,选项D不正确,答案选C。
本题难度:一般