时间:2017-09-24 01:18:27
1、选择题 25℃时,有浓度均为1 mol/L的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2三种溶液,若测得其中c(NH )分别为
)分别为
参考答案:
本题解析:
本题难度:一般
2、选择题 物质的量浓度相同的下列溶液中,符合pH由小到大顺序排列的是
A.Na2CO3 、NaHCO3、NaCl、NH4Cl
B.NaHCO3、Na2CO3 、NH4Cl、NaCl
C.NH4Cl、(NH4)2SO4、Na2S、NaNO3
D.(NH4)2SO4、NH4Cl、NaNO3、Na2S
参考答案:D
本题解析:Na2CO3 和NaHCO3属于强碱弱酸盐,水解显碱性,PH>7,NaCl属于强酸强碱盐,PH=7,NH4Cl属于强酸弱碱盐,PH<7,酸根离子对应的酸越弱,其盐水解能力越强,碱性越强,酸性H2CO3 >HCO3-,所以同浓度的.Na2CO3 和NaHCO3相比,Na2CO3碱性强,所以,pH由小到大顺序排列的是NH4Cl、NaCl、NaHCO3、Na2CO3,A,B项错误;(NH4)2SO4和NH4Cl都属于强酸弱碱盐,水解显酸性,(NH4)2SO4中NH4+ 的浓度大,水解产生的H+浓度大,PH最小,Na2S 属于强碱弱酸盐,水解成碱性,PH最大,pH由小到大顺序排列的是(NH4)2SO4、NH4Cl、NaNO3、Na2S,C项错误;D项正确;选D。
考点:考查溶液PH值的大小比较。
本题难度:一般
3、选择题 室温下,下列溶液中粒子关系关系正确的是
A.Na2CO3溶液:c(Na+)+c(H+)=c(H2CO3)+c(HCO3-)+c(OH-)+c(CO32-)
B.NaHSO3溶液:c(H+)+c(H2SO3)=c(HSO3-)+c(OH-)
C.KAl(SO4)2溶液:c(SO42-)>c(K+)>c(Al3+)>c(H+)>c(OH-)
D.NH4Cl和CaCl2混合溶液:c(Cl-)>c(Ca2+)>c(NH4+)>c(H+)>c(OH-)
参考答案:C
本题解析:Na2CO3溶液中电荷守恒:c(Na+)+c(H+)= c(HCO3-)+c(OH-)+2c(CO32-),故A项错误;NaHSO3溶液质子守恒:c(H+)+c(H2SO3)=c(SO32―)+c(OH-),故B项错误;KAl(SO4)2溶液存在离子为SO42-、K+、Al3+、H+、OH-,其中Al3+水解溶液呈酸性,故大小关系为:c(SO42-)>c(K+)>c(Al3+)>c(H+)>c(OH-),C项正确;NH4Cl和CaCl2混合溶液,但不知两者的相对大小,故不能确定Ca2+、NH4+的相对大小,D项错误。
考点:溶液中离子浓度关系。
本题难度:一般
4、填空题 (7分)
(1)在25℃条件下将pH=3的醋酸稀释100倍后溶液的pH为
A.5
B.1
C.1~3之间
D.3~5之间
(2)常温下,pH=3的盐酸和pH=11的氨水等体积混合后,混合溶液中
c(Cl-) c(NH4+)(填“>”、“=”或“<”)。
(3)常温下,已知某CH3COONa溶液中的c(Na+)=c(CH3COO一),则该溶液的pH 7(填“>”、“=”或“<”)。
(4)如果将NaOH和NH4Cl溶液等浓度、等体积混合,则混合溶液中各离子浓度由大到小的顺序为:c( ) c( ) c( ) c( ) c( )
[括号内填离子符号,“ ”上填写“>”或“=”]
(5)常温下等物质的量浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3・H2O;c(NH4+) 由大到小的顺序是:_____________________________(填序号)
参考答案:(共7分) (1)D(1分) (2)< (1分) (3)= (1分)
(4)c(Na+)=c(Cl--)>c(OH--)>c(NH4+)>c(H+)(2分) (5)①②③④(2分)
本题解析:(1)醋酸为弱酸,稀释会不断电离出氢离子,所以,pH=3的醋酸稀释100倍后溶液的pH为3~5之间;
(2)pH=3的盐酸和pH=11的氨水等体积混合后,因氨水为弱电解质,氨水过量,所以混合后溶液中的溶质为NH4CL、NH3・H2O;所以,混合溶液中c(Cl-)<c(NH4+);
(3)由电荷守恒可得c(Na+)+c(H+)=c(CH3COO一)+c(OH―);当c(Na+)=c(CH3COO一)时,溶液中c(H+)= c(OH―);即得该溶液的pH=7;
(4)因NH4+要发生水解,所以,c(Na+)=c(Cl--)>c(OH--)>c(NH4+)>c(H+);
(5)①由于AL3+水解溶液显酸性,会抑制NH4+的水解;③由于CH3COO―水解溶液显碱性,会促进NH4+的水解;所以,c(NH4+) 由大到小的顺序是:①②③④
本题难度:一般
5、填空题 根据下列要求写出有关反应式:
(1)钢铁发生吸氧腐蚀时,正极反应式:_____________________;
(2)用石墨作电极电解饱和食盐水的总反应:_____________________;
(3)将石墨接负极,铜板接正极,当通以直流电时,电解硫酸铜溶液,发生氧化反应的电极反应式:
_____________________ ;
(4)向明矾溶液中逐滴加入氢氧化钡溶液至硫酸根离子刚好沉淀完全时,离子反应方程式:
_____________________;
(5)蒸干AlCl3溶液,并灼烧。涉及到的化学反应方程式:_____________________。
参考答案:(1)2H2O+O2+4e-==4OH-
(2)2NaCl+2H2O 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
(3)Cu-2e-==Cu2+
(4)2Ba2++4OH-+Al3++2SO42-==2BaSO4↓+AlO2-+2H2O
(5)AlCl3+3H2O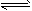 Al(OH)3+3HCl、2Al(OH)3
Al(OH)3+3HCl、2Al(OH)3 Al2O3+3H2O
Al2O3+3H2O
本题解析:
本题难度:一般