时间:2017-09-24 00:38:35
1、填空题 太阳能电池的发展已经进入了第三代。第一代为单晶硅太阳能电池,第二代为多晶硅、非晶硅等太阳能电池,第三代就是铜铟镓硒CIGS(CIS中掺人Ga)等化合物薄膜太阳能电池以及薄膜Si系太阳能电池。
(1)镓的基态原子的电子排布式是___?。
(2)硒为第4周期元素,相邻的元素有砷和溴,则3种元素的第一电离能从大到小顺序为?(用元素符号表示)。
(3)H2Se的酸性比H2S____(填“强”或“弱”)。气态SeO3分子的立体构型为____?。
(4)硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是?。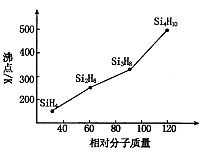
(5)与镓元素处于同一主族的硼元素具有缺电子性,其化合物往往具有加合性,因而硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]—而体现一元弱酸的性质,则[B(OH)4]—中B的原子杂化类型为?。
(6)金属Cu单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是____,反应的离子方程式为?。
(7)一种铜金合金晶体具有面心立方最密堆积的结构。在晶脆中,Au原子位于顶点,Cu原子位于面心,则该合金中Au原子与Cu原子个数之比为?,若该晶胞的边长为a pm,则合金的密度为?g·cm-3(已知lpm=10-12m,只要求列算式,不必计算出数值,阿伏加塞罗常数为NA)。
2、填空题 氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示; 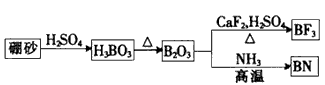
请回答下列问题:
(1)由B2O3制备BF3、BN的化学方程式依次是____、____;
(2)基态B原子的电子排布式为____;B和N相比,电负性较大的是________ ,BN中B元素的化合价为________ ;
(3)在BF3分子中,F-B-F的键角是__________ ,B原子的杂化轨道类型为_________ ,BF3和过量NaF作用可生成NaBF4, BF4-的立体构型为____;
(4)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为 ______,层间作用力为 _______;
(5)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5 pm。 立方氮化硼晶胞中含有____个氮原子、____个硼原子,立方氮化硼的密度是______ g·cm-3(只要求列算式,不 必计算出数值。阿伏加德罗常数为NA)。
3、选择题 下列表示物质结构的化学用语正确的是( )
A.氯化铵(NH4Cl)的电子式: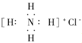
B.H2O2的电子式: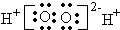
C.HClO的结构式:H-O-Cl
D.67166HO中的原子核内的中子数与核外电子数之差是99
4、填空题 写出下列物质的电子式:
(1)Ca(OH)2______,H2O______
(2)NH3______,MgO______,
(3)Na2O2______,CCl4______.
5、选择题 下列叙述一定正确的是
[? ]
A.在离子化合物中不可能存在非极性共价键
B.在共价化合物中不可能存在离子键
C.不同种非金属元素组成的多原于分子,其中的化学键一定全部是极性键
D.非极性键只存在于双原子单质的分子中