时间:2017-09-24 00:18:54
1、选择题 下列各组热化学方程式中,△H1>△H2的是
A.C(s)+O2(g)===CO2(g) △H1 C(s)+ ===CO(g)△H2
===CO(g)△H2
B.S(g)+O2(g)===SO2(g) △H1S(s)+O2(g)===SO2(g) △H2
C.2H2(g)+O2(g)===2H2O(l)△H1H2(g)+ ===H2O(l)△H2
===H2O(l)△H2
D.CaCO3(s)===CaO(s)+CO2(g)△H1 CaO(s)+H2O(l)===Ca(OH)2(s)△H2
参考答案:D
本题解析:A、碳不完全燃烧放热少,焓变比较大小考虑负号,所以△H1<△H2,故A不符合;B、固体硫变为气态硫需要吸收热量,故气体硫燃烧放出的热量多,焓变比较大小考虑负号,所以△H1>△H2,故B不符合;C、相同条件下物质的量少的反应放热少,焓变比较大小考虑负号,1mol氢气燃烧放热小于2mol氢气燃烧放热,所以△H1<△H2,故C不符合;D、碳酸钙分解吸热焓变为正值,氧化钙和水反应是化合反应放热,焓变是负值,所以△H1>△H2,故D符合;答案选D.
考点:反应热的大小比较
本题难度:一般
2、填空题 在电解炼铝过程中加入冰晶石(用“A”代替),可起到降低Al2O3熔点的作用。冰晶石的生产原理为2Al(OH)3+12HF+3Na2CO3=2Al+3CO2↑+9H2O。根据题意完成下列填空:
(1)冰晶石的化学式为?,含有离子键、?等化学键。
(2)生成物中含有10个电子的分子是?(写分子式),该分子的空间构型为?,中心原子的杂化方式为?。
(3)反应物中电负性最大的元素为?(填元素符号),写出其原子最外层的电子排布图:?。
(4)Al单质的晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。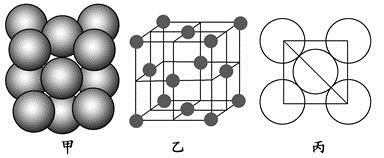
若已知Al的原子半径为d,NA代表阿伏加德罗常数,Al的相对原子质量为M,则一个晶胞中Al原子的数目为?;Al晶体的密度为?(用字母表示)。
参考答案:(1)Na3AlF6 配位键
(2)H2O V形 sp3
(3)F 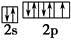
(4)4 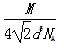
本题解析:(1)冰晶石的化学式为Na3AlF6,Na+与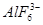 之间为离子键,而
之间为离子键,而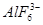 是以配位键形成的。(2)生成物中10电子分子是H2O,氧原子采取sp3杂化,由于氧原子含有两对孤电子对,故分子结构为V形。(3)F是电负性最大的元素,其最外层电子排布图为
是以配位键形成的。(2)生成物中10电子分子是H2O,氧原子采取sp3杂化,由于氧原子含有两对孤电子对,故分子结构为V形。(3)F是电负性最大的元素,其最外层电子排布图为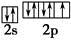 。(4)铝晶胞的原子处于晶胞顶角和面心,故一个晶胞含有的Al原子数目为6×
。(4)铝晶胞的原子处于晶胞顶角和面心,故一个晶胞含有的Al原子数目为6×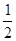 +8×
+8×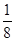 =4。设Al晶胞的边长为a,则有:2a2=(4d)2,a=2d,Al晶胞的体积为V=16d3,故Al晶体的密度为
=4。设Al晶胞的边长为a,则有:2a2=(4d)2,a=2d,Al晶胞的体积为V=16d3,故Al晶体的密度为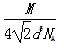 。
。
本题难度:一般
3、填空题 CH3-CH3→CH2=CH2+H2,有关化学键的键能如下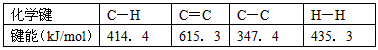
计算该反应的反应热_____________________
参考答案:+125.6 kJ/mol
本题解析:
本题难度:一般
4、选择题 下列物质中,含有非极性键的共价化合物是
A.CH3CH3
B.Na2O2
C.NaCl
D.N2
参考答案:A
本题解析:由同一种非金属元素的原子之间形成的化学键是非极性键,不同种非金属元素的原子之间形成的是极性键,据此可知,A中乙烷含有非极性键,B中含有非极性键,但是离子化合物,C中含有离子键,属于离子化合物,D中氮气是含有非极性键的单质,答案选A。
点评:该题是高考中的常见题型,属于基础性试题的考查。该题的关键是明确化学键的含义以及化学键和化合物的关系,然后结合题意灵活运用即可,有利于培养学生的逻辑推理能力,提升学生的学科素养。
本题难度:一般
5、选择题 下列各组离子,在pH=0的溶液中可以大量共存的是
A.Al3+、Fe3+、Br-、SO32-
B.K+、Na+、SO42-、NO3-
C.Na+、Cu2+、I-、NO3-
D.NH4+、K+、HCO3-、Cl-
参考答案:B
本题解析:分析:pH=0的溶液呈酸性,如离子之间不发生复分解、氧化还原反应或互促水解反应,则可大量共存,反之不能.
解答:A.酸性条件下Fe3+与SO32-发生氧化还原反应而不能大量共存,且SO32-与氢离子发生反应生成气体,故A错误;
B.离子之间不发生任何反应,可大量共存,故B正确;
C.酸性条件下I-、NO3-发生氧化还原反应而不能大量共存,故C错误;
D.酸性条件下HCO3-不能大量共存,故D错误.
故选B.
点评:本题考查离子共存问题,侧重于元素化合物知识的综合应用,为高考常见题型,注意把握相关离子的性质,注意题目酸性的特点,题目难度不大.
本题难度:一般