时间:2017-09-24 00:06:41
1、选择题 200mL0.1 mol・L-1CH3COOH与200mL0.1 mol・L-1NaOH溶液混合后,离子浓度关系正确的是
A.c(Na+)=c(CH3COO-)+c(CH3COOH)
B.c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
C.c(Na+)+c(OH-)= c(CH3COO-)+c(H+)
D.c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
参考答案:A
本题解析:200mL0.1 mol・L-1CH3COOH与200mL0.1 mol・L-1NaOH溶液混合后,相当于400mL0.1 mol・L-1CH3COONa溶液,A、正确,物料守恒,钠元素的总量与醋酸的各种存在形态相当;B、D不正确,CH3COO
本题难度:困难
2、选择题 下列溶液中,各微粒的物质的量浓度关系正确的是
A.室温下,向0.01 mol・L-1的NH4HSO4溶液中滴加NaOH溶液至中性:C(Na+)>C(SO42-)>C(NH4+)>C(OH-)=C(H+)
B.0.1 mol・L-1的NaHCO3溶液:C(Na+)>C(OH-)>C (HCO3-)>C(H+)
C.Na2CO3溶液:C(OH-)-C(H+)=C(HCO3-)+C(H2CO3)
D.25℃时,浓度均为0.1 mol・L-1的CH3COOH、CH3COONa混合溶液,呈酸性:C(CH3COO-)+C(OH-)<C(CH3COOH)+C(H+)
参考答案:A
本题解析:A、室温下,向0.01 mol・L-1的NH4HSO4溶液中滴加NaOH溶液至中性,则C(OH-)=C(H+),且满足电荷守恒,2C(SO42-)+C(OH-)=C(H+)+ C(Na+)+ C(NH4+),2C(SO42-)=C(Na+)+ C(NH4+)则若二者等物质的量反应,则生成硫酸钠、硫酸铵,溶液呈酸性,所以溶液呈中性时,氢氧化钠稍过量,则C(Na+)> C(SO42-),同理C(SO42-)> C(NH4+),正确;B、碳酸氢钠溶液呈碱性,则溶液中的两种浓度的关系为C(Na+)>C (HCO3-)>C(OH-)>C(H+),错误;C、碳酸钠溶液中,根据质子守恒,可得C(OH-)=C(H+)+C(HCO3-)+2C(H2CO3),即C(OH-)-C(H+)=C(HCO3-)+2C(H2CO3),错误;D、25℃时,浓度均为0.1 mol・L-1的CH3COOH、CH3COONa混合溶液,呈酸性,说明醋酸的电离程度大于醋酸根离子的水解程度,所以C(CH3COO-)> C(Na+)>C(CH3COOH)> C(H+)> C(OH-),根据电荷守恒有C(H+)+ C(Na+)=C(CH3COO-)+C(OH-)> C(CH3COOH)+C(H+),错误,答案选A。
考点:考查电解质溶液中离子浓度关系的判断
本题难度:困难
3、选择题 水中加入下列溶液对水的电离平衡不产生影响的是( )
A.NaHSO4溶液
B.KF溶液
C.KAl(SO4)2溶液
D.NaI溶液
参考答案:D
本题解析:A项中电离出的H+抑制水的电离;B项中F-水解促进水的电离;C项中Al3+水解促进水的电离;D项中NaI为强酸强碱盐,对水的电离无影响
本题难度:一般
4、选择题 下列说法正确的是( ? )
 MgCl2+6H2O
MgCl2+6H2O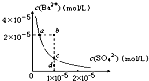
参考答案:B
本题解析:
本题难度:一般
5、选择题 以下有关溶液(均在常温下)的结论正确的是
A.pH=1的盐酸与pH=5的盐酸等体积混合后pH=3
B.0.1 mol/L醋酸溶液100 mL与0.2 mol/L氨水50 mL混合后能恰好完全中和
C.pH>7的溶液中不可能存在CH3COOH分子
D.等浓度等体积的KOH溶液和CH3COOH溶液混合后:c(CH3COO-)=c(K+)
参考答案:B
本题解析:A项pH=1的盐酸与pH=5的盐酸等体积混合后pH约等于1.3;C项如CH3COONa溶液,由于水解pH>7,但溶液中存在CH3COOH分子;D项等浓度等体积的KOH溶液和CH3COOH溶液混合后c(CH3COO-)<c(K+)。
考点:水的电离,溶液的pH
本题难度:一般